Unutar hemije postoji bezbroj elemenata koji mogu biti ili ne moraju biti povezani jedni s drugima. Postoje metali, nemetali, lantanidi i aktinidi, prelazni metali i zemnoalkalne zemlje; i naravno da jesmo jedan od hemijskih elemenata Kome smo obraćali malo pažnje na časovima hemije, a mnogo manje kada je u pitanju nastavak našeg života. Govorim, naravno, o plemenitim plinovima.
Ovi elementi koje, budući da su toliko rijetki u okolini, ne možemo previše analizirati. Ovdje ćemo naučiti o povijesti plemenitih plinova, njihovoj upotrebi i svojstvima, kao i drugim zanimljivostima. Ostanite ovdje i naučite najhladnije stvari o plemenitim plinovima.
Upoznajmo plinove
Oni su grupa hemijskih jedinjenja koja imaju vrlo slična svojstva. Na primjer, u normalnim su uvjetima monatomski plinovi bez boje, mirisa i vrlo niske hemijske reaktivnosti. Oni se nalaze u grupi broj 18 periodnog sistema i poznati su kao: Helij, neon, ksenon, argon, kripton, radioaktivni: Radon i sintetički: Oganeson.
Njegova svojstva mogu se objasniti postojećim modernim teorijama o atomskoj strukturi. Njihova valentna elektronska ljuska smatra se potpunom, što im daje ograničenu tendenciju da učestvuju u hemijskim reakcijama, i jedan je od razloga zašto su slabo razumljivi. Zapravo je do danas pripremljeno vrlo malo spojeva plemenitih gasova.
Odakle nam plemeniti plinovi?
Neon, argon, ksenon i kripton dobivamo iz vazduha metodom frakcione destilacije i ukapljivanja. Helij se nalazi u prirodnom plinu, gdje bi trebao biti tipično odvojen. A radon se dobija radioaktivnim raspadanjem jedinjenja rastvorenih u radijumu.
A Oganeson je sintetički element stvoren 2002. godine i koji je svoju IUPAC-ovu nomenklaturu dobio 2016. Poznat je po tome što je prilično reaktivan, ali i nestabilan, pa se s njim nije puno radilo.
Ovi plinovi su imali vrlo važnu upotrebu na polju osvjetljenja, zavarivanja i istraživanja svemira. Trimix, koji je otopina helij-kiseonik-azot, koristi se u tome da ronioci ne trpe narkotično dejstvo dušika u dubinama. Šta više, nakon poznavanja opasnosti zapaljivosti vodonika, ovo je zamijenjeno helijem u stvaranju zračnih brodova i balona s vrućim zrakom.
Svojstva ovih gasova
Plemeniti plinovi ime su dobili po prijevodu s njemačkog edelgas, ime koje je prvi put 1898. godine upotrijebio kemičar Hugo Erdman. Sa ovim imenom nastojalo da se odnosi na nisku stopu reaktivnosti ovih elemenata. Zapravo su to najmanje poznati reaktivni elementi, toliko da su praktički inertni ili nereaktivni.
To je zbog činjenice da imaju potpunu valentnu ljusku koja im ostavlja mali kapacitet za oslobađanje elektrona i njihovo ponašanje približava ponašanju idealnog plina.
Općenito, plemeniti plinovi dijele različita svojstva.
- Oni su nemetalni elementi: Budući da je plin, u svojoj konformaciji nema nijedne metalne čestice. Istovremeno nisu sposobni za reakciju s drugim metalima.
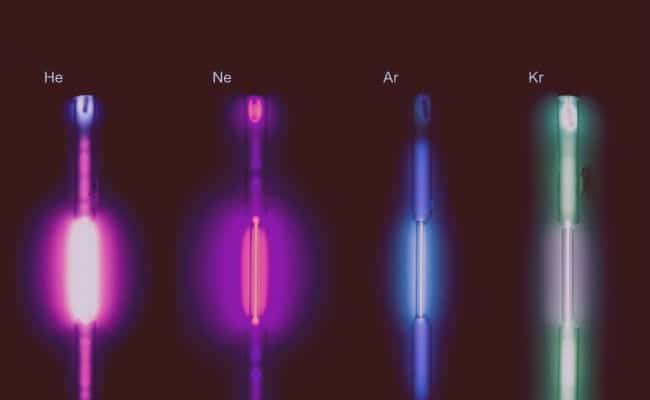
- Bez boje su i bez mirisa: iako se mogu dati boje sijalica i lampi stvoreni pomoću ovih plinova koji koriste električnu energiju, izvorno su bez boje i mirisa.
- Imaju puni valentni sloj: Neon, ksenon, argon, kripton i radon imaju osam elektrona u posljednjoj ljusci. Sa svoje strane, helij ima dva elektrona. Na taj način plemeniti plinovi imaju potpunu valentnu ljusku. Zbog toga, u normalnim okolnostima, ovi elementi ne čine veze.
- Postoje kao monatomski plinovi: Kako se razumije, ovi elementi, čak i najveći atomski, imaju samo jedan atom.
- Oni su praktično nereaktivni: Zbog njihove pune valencije i poteškoća u isporuci elektrona, smatraju se praktično inertnim.
- Oni provode električnu energiju i proizvode fluorescenciju: Iako su vrlo niski, ovi plinovi su sposobni provoditi električnu energiju i pritom svijetle fosforescentno.
- Imaju nisku tačku topljenja i ključanjaOvi plemeniti plinovi imaju vrlo niske tačke topljenja i ključanja.
- Imaju vrlo nisku elektronegativnost: ovi elementi su vrlo nisko elektronegativni
- Imaju visoku energiju jonizacije: Vaša energija jonizacije je zapravo najviša u vašem periodu.
- Nisu zapaljive: Čak i zbog zapaljive čaše vodika, u proizvodnji zračnih brodova i balona zamijenio ga je helij.
Kao i kod reaktivnosti, njihove međuatomske sile također su vrlo slabe, zbog čega imaju niske temperature topljenja i ključanja, a svi su oni monatomski plinovi u normalnim uvjetima, uključujući plinove veće atomske mase.
Helij ima mnoga svojstva koja nema nijedan drugi plemeniti plin ili bilo koji drugi element na periodnom sustavu. Njegov tačka topljenja je najniža u svim poznatim, osim što je jedini element koji posjeduje stanje supertečnosti; stanje u kojem je materija u tečnom stanju, ali može raditi bez gubitka kinetičke energije. Helijumu je potreban pritisak od 25atm i temperatura od -272ºC da bi se stvrdnuo.
Njihova puna valentna ljuska odgovorna je i za ove plinove koji imaju visoku sposobnost jonizacije (najveći u periodnom sustavu). i ne mogu lako stvoriti jone, što pokazuje njegovu stabilnost u elektroničkoj konfiguraciji.
Energija jonizacije se smanjuje kako se grupa smanjuje, jer se atomski radijus povećava, a valentni elektroni su dalje od jezgre i zbog toga je manje privlače. To uzrokuje da, iako je njegovo razdoblje najviše, imaju neki plemeniti plinovi uporediva energija jonizacije onom ostalih elemenata. Na primjer, energija jonizacije ksenona usporediva je sa energijom jonizacije kiseonika.
Upotreba ovih gasova
Imajući tako niske tačke ključanja i topljenja, posebno su korisni u proizvodnji rashladne opreme, te ih čini korisnima i kao kriogena rashladna sredstva.
Tečni helij koji ključa na 4,2K (-268,93ºC) koristi se u proizvodnji superprovodljivih magneta, poput onih koji se koriste za magnetnu rezonancu i nuklearnu magnetnu rezonancu.
Tekući neon, iako ne doseže niske temperature tečnog helijuma, ima više primjena u kriogenici, jer ima sposobnost da 40 puta više hlađenja od tečnog helijuma i 3 puta veća od one u tečnom vodoniku.
Helij se koristi kao komponenta prozračnih plinova za zamjenu dušika, zahvaljujući njegovom niska rastvorljivost u tečnostima, posebno u lipidima. Plinovi se apsorbiraju u krv i tjelesna tkiva kada postoji pritisak, poput ronjenja, koje proizvodi anestetički efekt koji se naziva dubinska bolest. Zbog niske topljivosti, malo helija ulazi u ćelijske membrane, što pomaže u suzbijanju narkotičnog učinka.
Zbog niske zapaljivosti i lakoće, te nakon katastrofe u Hindenburgu 1937. godine, helij je zamijenio vodik u proizvodnji goriva, čak i uprkos gubitku uzgona od 8,6%
Ovi plinovi se koriste u rasvjeti zbog svoje provodljivosti. U proizvodnji žarulja sa žarnom niti koristi se mješavina argona i azota za njihovo punjenje. Kripton koristi se u sijalicama visokih performansikao što su halogene lampe, koje imaju višu temperaturu boje i veću efikasnost.
Ksenon se obično koristi u ksenonskim farovima, koji se postizanjem svjetlosnog spektra sličnog dnevnom, koriste u filmskim projektorima, kao i u automobilskim svjetlima.
U medicini se helij koristi za poboljšanje lakoće disanja kod pacijenata sa astmom. Ksenon se može koristiti kao anestetik Zbog visoke topivosti u lipidima, što ga čini učinkovitijim od uobičajenog dušikovog oksida, a budući da ga tijelo lako uklanja, omogućava brži oporavak.
Snimanje slika koje se vrši nuklearnom magnetnom rezonancom ima ksenon u kombinaciji sa drugim gasovima. Radon, koji je visoko radioaktivan i dostupan je samo u tragovima, koristi se u terapiji zračenjem.
Proizvodnja i obilje
Obilje i lakoća s kojima se mogu dobiti plemeniti plinovi u obrnutom su srazmjeru sa njihovim atomskim brojem. Stoga se obilje ovih plinova smanjuje kako njihov atomski broj raste.
U svemiru, helij je drugi element koji je najlakše dobiti, nakon vodonika, sa masenim procentom od približno 24%. Većina količine helijuma u svemiru nastala je primordijalnom nukleosintezom, ali njegova količina se povećava zahvaljujući sudjelovanju vodonika u zvjezdanoj nukleosintezi (proces koji nastaje nuklearnim reakcijama tokom evolucijskog procesa zvijezda).
Ostatak plinova nije ni izdaleka ni jednostavan za dobivanje. Radon, na primjer, može biti oblik u litosferi kroz alfa raspadanje radijuma; U međuvremenu on ksenon je razvio teoriju poznatu kao "teorija ksenona koja nedostaje" zbog relativno male količine u atmosferi.
Razgovarajmo malo o svakom
- sunce: Zbog svoje male zapaljivosti i jer je drugi element koji je najlakše dobiti, uspio je zamijeniti vodik kao potencijalni element za punjenje balona i cepelina, jer ne eksplodiraju kada dođu u kontakt s vatrom.
- Neon: Ovaj plin se zbog svoje fluorescencije i crveno-narančaste nijanse dobivene u kontaktu s električnom energijom koristi u reklamne svrhe. Lako se nalazi u neonskim svjetlima. Možete dobiti i neonske cijevi i lampe koje imaju druge boje, iako one zapravo imaju druge plinove unutra.
- Argon: Ovaj se plin koristi u žaruljama sa žarnom niti, jer ne reagira sa žarnom niti u uvjetima visoke temperature i pritiska. U fluorescentnim cijevima stvara zeleno-plavu boju. Takođe se koristi u industrijskom polju kako bi se izbegle neželjene hemijske reakcije.
- Kripton: Koristi se zajedno s ostalim plinovima u stvaranju i proizvodnji svjetiljki osvjetljenje aerodroma, zbog intenziteta emitiranih crvenih svjetala; može se koristiti i u bioskopskim projektorima. Upotreba kriptona korisna je i u laserskoj operaciji mrežnjače.
- Xenon: glavna upotreba ksenona je izrada emitora svjetlosti sa baktericidnim karakteristikama; svjetleće cijevi, fotografski bljeskovi, a također i u fluorescentnim cijevima sa sposobnošću pobuđivanja rubin lasera.
- Radon: Ovaj plin nastaje radioaktivnim raspadanjem urana na radio. Zbog toga i zato što je vrlo radioaktivan, ima vrlo malo primjena u svakodnevnom životu.
Da razmislim
Iako su donekle sastavljeni teško je dobiti u prirodnom stanju (osim možda helija), a budući da s njima generiraju ili dopuštaju vrlo malo reakcija, plemeniti plinovi su važni spojevi koje možemo vidjeti, pa čak i svakodnevno koristiti.
Možda su njihove upotrebe ograničene na određena polja, ali to ne znači da su potpuno beskorisne. Od osvjetljavanja domova u sijalicama i lampama, preko držanja hrane kada se koristi u hladnjacima, spasiti živote kada se koristi u mediciniOvi plinovi, prirodni ili sintetički, još nisu pokazali sve što mogu učiniti za nas. I sigurno je da će, kako istraživanja budu odmicala, njegova upotreba biti sve veća.
Koja je sposobnost jonizacije?
i njegova krhkost