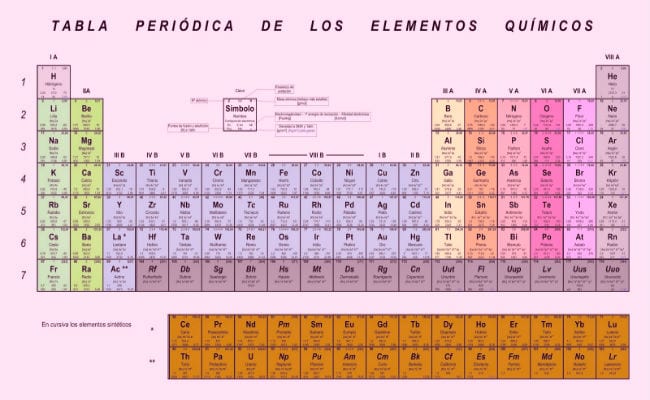
Jedno od velikih dostignuća na naučnom nivou bila je klasifikacija i organizacija elemenata. Proučavanje svojstava materije datira još iz vremena alhemičara, znanstvenici ovog područja uvijek su imali na umu važnost uspostavljanja sustava klasifikacije, koji bi omogućio uredno upravljanje elementima koji su bili poznati u to vrijeme.
Odatle je, nakon mnogih pokušaja, razvijena poznata tablica elektronegativnosti, poznata i kao Mendelejev periodni sistem, što je najefikasniji sistem klasifikacije i organizacije koji imamo do sada. U njemu su raspoređeni elementi funkcija njihovih elektronegativnosti, što je mjera sposobnosti elektrona njegove posljednje ljuske da se kombiniraju s drugim atomima, ali o tome ćemo razgovarati.
Šta je elektronegativnost?
Prije nego što u potpunosti pređemo na temu, važno je razjasniti da se sva materija sastoji od atoma, kako je to definirao John Dalton 1803. Atom je elementarna i nedjeljiva jedinica materije koja se sastoji od jezgre, oko koje elektroni i protoni se okreću u eliptičnim orbitama, a to su elektroni prisutni u posljednjem sloju elementa u agregatnom stanju određuje kapacitet svakog materijala da se formiraju jedinjenja. To je ono što definiše elektronegativnost, sposobnost atoma da se kombinuje kroz veze sa drugim atomima.
Ovaj postupak je definiran djelovanjem dvije veličine:
- Atomska masa: Kolika je ukupna masa protona i neutrona u jednom atomu.
- Valentni elektroni: Negativno nabijene čestice smještene u posljednjem sloju atoma, koje čine količinu čestica dostupnih za obavljanje razmjene u stvaranju spojeva.
Razvoj tablice elektronegativnosti
U potrazi za adekvatnom klasifikacijom elemenata, mnogi su naučnici razvili ideje oko toga što bi mogao biti prikladan sistem, putem kojeg bi se elementima moglo pristupiti uredno, uzimajući u obzir njihova svojstva. Sljedeći naučnici dali su važan doprinos razvoju trenutne tabele elektronegativnosti:
- Antoine Lavoisier: Klasifikacija elemenata koju je izvršio ovaj naučnik izvršena je proizvoljno, ne uzimajući u obzir bilo koji kriterij klasifikacije, tako da njegova klasifikacija nije bila previše uspješna.
- Johann Doberiner: Ovaj naučnik poznat je po razvoju trijada koje nose njegovo ime. Razvio je studiju u kojoj je elemente grupirao u grupu od troje, uspoređujući uspoređujući da je njihova relativna atomska masa (koji se određuju pomoću masenog spektrometra), a određene vrijednosti njihovih fizičkih svojstava bile su međusobno povezane. Stoga bi ih se moglo predvidjeti matematičkim aproksimacijama. Britanski kemičar John newlands, radio na osnovi koju je razvio Dobereiner, i tako uspio poredati elemente u tablici s grupisanjem elemenata relativne atomske mase u sve većem obliku; Ovim grupiranjem, Britanci su pokušali razviti tablicu u kojoj se nalazi obrazac periodičnog ponavljanja fizička svojstva elemenata. Budući da su takva ponavljanja grupirana oko 8 elemenata, označena su imenom "Zakon oktave".
- Lothar Mayer: Poznat je po širenju znanja u polju proučavanja odnosa fizičkih svojstava i atomskih svojstava komponenata. Njegov rad je bio komplementaran i, zauzvrat, neovisan od djela koje je proizveo Mendeleev.
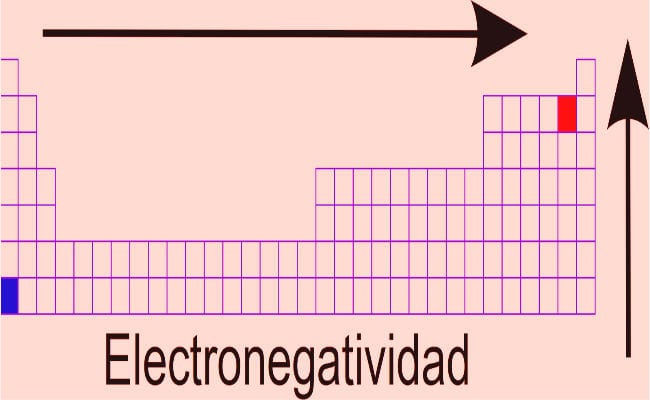
- Dmitri Mendeleev: Na osnovu postulata periodični zakon, ovaj je znanstvenik razvio najuspješniji rad na klasifikaciji elemenata koji je i dalje na snazi (s izmjenama u koje su dodani novi otkriveni elementi. Elemente je klasificirao uzimajući u obzir njihovu elektronegativnost i imao je viziju ostavljanja kutija u kojima nema elemenata fit, predviđajući da će tu stati element koji još nije otkriven. Poznati elementi koji su izbjegli parametre reda zabilježeni su odvojeno, umjesto da budu proizvoljno uključeni (grešku napravili Lavoisier i Newlands). Što se tiče elektronegativnosti u tablici, opće je pravilo: Elektronegativnost je vrijednost koja se povećava kako se pomičemo udesno od stola, primjećujući smanjenje pri kretanju ulijevo. Elementi na vrhu tablice imaju veće vrijednosti elektronegativnosti.
Vage elektronegativnosti
Različite vrijednosti elektronegativnosti određuju vrstu nastale veze, pa je proučavanje ovog procesa bilo predmet interesa, a razvijena su dva postulata:
Pauling skala: Prema Paulingovim studijama ustanovljeno je da je elektronegativnost promjenjivo svojstvo, jer ovisi o oksidacijskom stanju elementa. Njegova zapažanja omogućila su mu da utvrdi da, ako se izvrši oduzimanje ili razlika elektronegativnosti, možemo predvidjeti vrstu veze koja će se stvoriti, budući da je uspostavio skalu:
- Jonska veza: Gradijent elektronegativnosti veći ili jednak 1.7. Ova veza se obično javlja između metalnih i nemetalnih elemenata.
- Kovalentna veza: Kada je razlika u rasponu od 1.7 do 0.4. Uobičajeno ih je vidjeti u nemetalnim spojevima.
- Polarni link: Za razlike jednake ili manje od 0.4.
Mulliken skala: Zasnovan je na elektroničkom afinitetu elemenata, koji definira njihovu tendenciju da steknu negativan naboj, što definira sposobnost elementa da prihvati elektrone. Takođe radi s jonskim potencijalima, koji zauzvrat određuju predispoziciju elementa da preuzme pozitivan naboj (pozitivno nabijeni elementi su oni koji doniraju elektrone iz svoje posljednje ljuske). Ova skala radi sa prosječnim vrijednostima.