Sigurno ste ikada čuli za kristale, vjerojatno je u ovom trenutku vaš um vizualizirao ogroman dijamant, ametist ili topaz. I svakako, u ovu grupu spadaju i mnogi poznati "Drago kamenje", ali kristal nije naziv koji jasno obuhvaća područje nakita.
Kristal je krajnji proizvod zanimljivog procesa poznatog kao kristalizacija, koji se karakterizira rezultiranjem homogenom čvrstom supstancom koju čine "lica", a to su dijelovi smješteni u različitim ravnima.
Karakteristike čvrste supstance iz kristalizacije
Veličina kristala je promjenjiva karakteristika, u širokom rasponu dimenzija. Mogu se naći "ogromni" kristali koji se mogu mjeriti kao i mi pomoću linearne jedinice "metar" pronađi kristale to mora biti izraženo u terminima "mikrona", jer ih mala veličina čini uporedivima s mikroorganizmima poput bakterija, koji su vidljivi samo kroz mikroskop.
Kao što je spomenuto, kristalni procesi rezultiraju proizvodima visoke čistoće, zato smo to ranije u definiciji i utvrdili kristali su homogeni: to jest, sastav proizvoda ostaje na konstantnoj vrijednosti u bilo kojem trenutku volumena krutine, što također podrazumijeva da fizičke i kemijske karakteristike ostanu nepromijenjene u cijelom komadu, au slučaju uočavanja varijacija uslijed poremećaja, promjena će se dogoditi u cijeloj vrsti. Ova kvaliteta čini kristale vrijednim proizvodima u raznim poljima, u rasponu od ocjene kvalitete materijala do upotreba procesa kristalizacije kao tehnike za odvajanje supstanci.
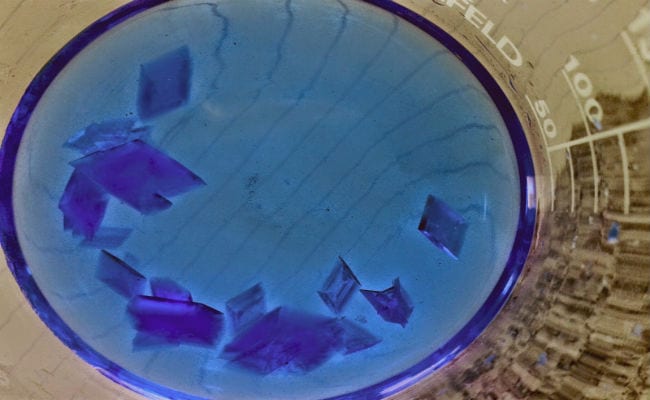
Kristalni proizvodi se takođe mogu izolirati na laboratorijskoj razini, kontroliranim reakcijama u sklopovima koji oponašaju spontane procese koji se javljaju u prirodi. Jedna od glavnih prednosti kristala dobivenih u kontroliranim procesima je u tome što predstavljaju pravilnije oblike, koji savršeno odgovaraju poligonalnim figurama veće preciznosti.
U kristalu moramo razlikovati lica koja su dio stvarne kristalne navike (morfološke karakteristike), a na osnovu njihovog broja možemo razmotriti temeljne oblike krutine. Obično u kristal se definira kombinacijom nekoliko osnovnih oblika, od kojih su glavni sljedeći:
- Pedion: Staklo koje se sastoji od jednog ravnog lica, bez ekvivalenata.
- Pinakoid: Sastoji se od dvije ekvivalentne plohe u odnosu na osu simetrije.
- Sfenoid: Dvije ekvivalentne plohe koje čine ovaj čvrsti materijal leže oko binarne osi.
- Prizma: Čine ga homologna lica koja čine zonu. Budući da je "područje kristala" definirano kao skup lica paralelnih istom smjeru, koji odgovaraju ivici istog.
Strukturu kristala s unutarnje točke gledišta možemo smatrati sastavljenom više ili manje homogenim, periodičnim i anizotropnim sustavom otopljenog materijala koji razvija strukturu u različitim točkama u prostoru. Unutar karakteristika kristala, zanimanje je uvijek pobuđivala činjenica da svaka točka redovno ponavljati u prostoru koji zauzima materijal. U kristalografiji se naziva fenomen koji utječe na ovu akciju prijevod.
Proces kristalizacije
Da bi došlo do kristalizacije, moramo poći od supstance koja se može klasificirati kao "Kristalno", i to je definirano jer čestice koje ga čine, bilo da su atomske, molekularne ili jonske prirode, imaju svojstva homogenosti, periodičnosti i simetrije.
Čitav proces se aktivira kada se u nekom trenutku u kristalnoj supstanci čestice počnu reorganizirati, u fazi poznatoj kao nukleacija. Čitav ovaj proces uključuje, pored evidentne promjene u redoslijedu čestica, i proces promjene termodinamičkih uvjeta koji su orijentirani na kompenzaciju poremećaja nastalih promjenom Gibbsove slobodne energije, što je označeno s tri događaji:
- Promjena hemijske energije.
- Stvaranje veze između zone nukleacije i ostatka homogene faze.
- Varijacije u volumenu i obliku koje ovaj proces uključuje pokreću napetosti.
Sljedeća faza nastaje kada se struktura baze nukleacije stabilizira. Sljedeći korak je nešto logično i predvidljivo, nakon što imamo osnovnu strukturu ući ćemo u proces rast, u kojem se uočava promjena dimenzija jezgre. Malo po malo, ovo povećanje rezultirat će stvaranjem lica, sve dok kristal ne stekne dobro definiranu naviku.
Mehanizam rasta kristala
Teorija koju je razvio Volmer objašnjava kako se odvija rast kristala, utvrđujući da je, oko osnovne strukture iz nukleacije kristalne supstance, vrsta upijajući sloj, koji djeluje kao sučelje, a uz to, pospješuje migraciju čestica oko sebe, koje se kreću paralelno s površinom. Rezultat ovog procesa definiran je kao struktura definirana u dvodimenzionalnoj ravni.
Sa svoje strane, Kossel i Straski su to utvrdili potreban je mehanički rad kako bi se postigla fiksacija jona na površinu ovog sloja i da to ovisi o njegovom položaju.
Razvoj modela koji definira rast zahtijeva prognozu zona zasićenja gdje se uočava veća brzina promjena (lokalne zone prezasićenja). To pokazuje da se rast kristala događa u slojevima.
Kristalizacija kao mehanizam razdvajanja
Budući da je kristal nastao sa homogenom supstancom, njegova upotreba kao metoda selektivnog odvajanja supstanci proširena je, među nekoliko metoda, u nastavku, objasnit ćemo od čega se sastoje oni čija je upotreba rasprostranjenija:
- Dodavanje novog rastvarača: Ako znamo prirodu proizvoda s kojima rukujemo, možemo primijeniti ovu metodu koja se u osnovi sastoji od dodavanja novog otapala koje stupa u interakciju s otapalom u kojem je otopljena otopljena tvar koja želimo kristalizirati. Kada novo otapalo selektivno počne komunicirati sa svojim homologom, otopljena supstanca se taloži, započinjući proces kristalizacije.
- Hlađenje do visokih koncentracija otopljene supstance: Kada imamo otopinu visoke koncentracije koja je napravljena na visokim temperaturama i podvrgnemo je procesu hlađenja, dobivamo stanje prezasićenja, u kojem je otopljena veća količina otopljene supstance nego što otapalo može prihvatiti, u tim novim temperaturni uslovi. Ako se postupak smanjenja temperature vrši na kontroliran način, možemo utjecati na veličinu kristala koji ćemo dobiti.
- Sublimacija: Ova tehnika može se primijeniti samo u kristalnim spojevima koji predstavljaju visok pritisak pare, na takav način da transformacije iz plinske faze u čvrstu ne zahtijevaju prolazak kroz tačku topljenja.