Keemia sees on lugematu arv elemente, mis võivad olla üksteisega seotud või mitte. On metalle, mittemetalle, lantaniide ja aktiniide, siirdemetalle ja leelismuldi; ja muidugi meil on üks keemilistest elementidest Kellele oleme keemiatundides vähe tähelepanu pööranud ja palju vähem oma eluga edasi liikumisel. Ma räägin muidugi üllastest gaasidest.
Neid elemente, mida keskkonnas on nii harva, ei saa me liiga palju analüüsida. Siit saame teada väärisgaaside ajaloost, nende kasutamisest ja omadustest ning muudest kurioosumitest. Jääge siia ja õppige väärisgaaside kohta kõige lahedamaid asju.
Tutvume gaasidega
Need on keemiliste ühendite rühm, millel on üksteisega väga sarnased omadused. Näiteks on need normaalsetes tingimustes värvusetud, lõhnatud, monatoomilised gaasid ja nende keemiline reaktsioonivõime on väga madal. Need asuvad perioodilise tabeli rühmas 18 ja on tuntud kui: Heelium, neoon, ksenoon, argoon, krüpton, radioaktiivne aine: radoon ja sünteetiline aine: Oganeson.
Selle omadusi saab seletada olemasolevate kaasaegsete aatomistruktuuri teooriatega. Nende valentsete elektronide kesta peetakse täielikuks, mis annab neile piiratud kalduvuse osaleda keemilistes reaktsioonides ja see on üks põhjus, miks neid halvasti mõistetakse. Tegelikult on tänapäevani valmistatud väga vähe väärisgaasi ühendeid.
Kust saame väärisgaasid?
Neooni, argooni, ksenooni ja krüptooni saame õhust fraktsioneeriva destilleerimise ja veeldamise meetodite abil. Heeliumi leidub maagaasis, kus see peaks tavaliselt olema eraldatud. Ja radoon saadakse raadiumis lahustunud ühendite radioaktiivse lagunemise kaudu.
Ja Oganeson on sünteetiline element, mis loodi 2002. aastal ja mille IUPAC-i nomenklatuur sai 2016. aastal. See on tuntud nii üsna reaktiivse kui ka ebastabiilse toimega, mistõttu pole sellega palju tööd tehtud.
Nendel gaasidel on olnud väga oluline kasutusala valgustuse, keevitamise ja kosmoseuuringute valdkonnas. Trimixi, mis on heeliumi-hapniku-lämmastiku lahus, kasutatakse selleks, et sukeldujad ei kannataks sügavuses lämmastiku narkootilist toimet. Mis veel, pärast vesiniku tuleohtlikkuse teadmist, see asendati õhulaevade ja kuumaõhupallide loomisel heeliumiga.
Nende gaaside omadused
Väärisgaasid saavad oma nime tõlkes saksa keelest edelgas, nime kasutas keemik Hugo Erdman esmakordselt 1898. aastal. Selle nimega püüdis viidata madalale reaktsioonikiirusele nendest elementidest. Tegelikult on need teadaolevalt kõige vähem reageerivad elemendid, nii et nad on praktiliselt inertsed või mittereaktiivsed.
Seda seetõttu, et neil on täielik valentskest, mis jätab neile madala võime vabastada elektrone ja muudab nende käitumise ideaalse gaasi lähedaseks.
Üldiselt on väärisgaasidel erinevad omadused.
- Need on mittemetallilised elemendid: Gaasidena ei ole selle konformatsioonis ühtegi metallosakest. Samal ajal ei ole nad võimelised reageerima teiste metallidega.
- Need on värvusetud ja lõhnatud: kuigi neid saab anda pirnide ja lampide värvid nende gaaside abil, mis kasutavad elektrit, on need algselt värvusetud ja lõhnatud.
- Neil on täielik valentsikiht: Neooni, ksenooni, argooni, krüptooni ja radooni viimases kestas on kaheksa elektroni. Heeliumil on omalt poolt kaks elektroni. Sel moel on väärisgaasidel täielik valents kest. Seetõttu ei moodusta need elemendid tavaolukorras linke.
- Need eksisteerivad monatoomiliste gaasidena: Nagu aru saadakse, on nendel elementidel, isegi aatomi poolest suurimatel, ainult üks aatom.
- Need ei ole praktiliselt reageerivad: Nende täieliku valentsuse ja raskuste tõttu elektronide edastamisel peetakse neid praktiliselt inertseteks.
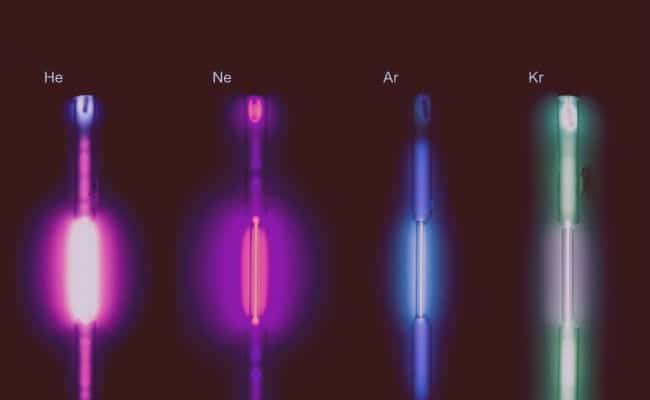
- Nad juhivad elektrit ja toodavad fluorestsentsi: Kuigi need gaasid on väga madalad, on need võimelised juhtima elektrit ja seda tehes hõõguvad fosforestseeruvalt.
- Neil on madal sulamis- ja keemistemperatuurNendel väärisgaasidel on väga madal sulamis- ja keemistemperatuur.
- Neil on väga madal elektronegatiivsus: need elemendid on väga madala elektronegatiivsusega
- Neil on kõrge ionisatsioonienergia: Teie ionisatsioonienergia on tegelikult teie perioodi kõrgeim.
- Need ei ole tuleohtlikud: Isegi süttiva vesinikutassi tõttu asendati see õhulaevade ja õhupallide valmistamisel heeliumiga.
Nagu reaktiivsuse korral, on ka nende aatomitevahelised jõud väga nõrgad, mistõttu neil on madalad sulamis- ja keemistemperatuurid ning nad on kõik normaalsetes tingimustes monatomilised gaasid, sealhulgas suurema aatommassiga gaasid.
Heeliumil on palju omadusi, mida pole ühelgi teisel väärisgaasil ega mõnel muul perioodilisustabeli elemendil. Tema oma sulamistemperatuur on madalaim kõigis teadaolevates, lisaks sellele, et see on ainus element, millel on ülivedeliku seisund; olek, kus aine on vedelas olekus, kuid võib kulgeda kineetilist energiat kaotamata. Tardumiseks vajab heelium rõhku 25atm ja temperatuuri -272ºC.
Nende täisvalentsuskest vastutab ka selle eest, et need gaasid omaksid suurt ionisatsioonivõimet (perioodilisustabeli kõrgeim). ja ei saa kergesti ioone moodustada, mis näitab selle stabiilsust elektroonilises konfiguratsioonis.
Ionisatsioonienergia grupi vähenemisega väheneb, kuna aatomi raadius suureneb ja valentselektronid on tuumast kaugemal ja seetõttu tõmbuvad selle poole vähem. See põhjustab, et kuigi selle periood on kõige kõrgem, on mõnel väärisgaasil seda võrreldav ionisatsioonienergia muude elementide omaga. Näiteks on ksenooni ionisatsioonienergia võrreldav hapniku ionisatsioonienergiaga.
Nende gaaside kasutamine
Selliste madalate keemis- ja sulamistemperatuuridega need on eriti kasulikud külmutusseadmete valmistamiselja muudab need kasulikuks ka krüogeensete külmutusagensitena.
Vedelat heeliumi, mis keeb temperatuuril 4,2 K (-268,93 ° C), kasutatakse ülijuhtivate magnetite valmistamiseks, näiteks magnetresonantstomograafia ja tuumamagnetresonantsi jaoks.
Vedel neoon, kuigi see ei saavuta vedelat heeliumi madalat temperatuuri, on krüogeenikas rohkem kasutatav, kuna see on võimeline 40 korda rohkem jahutust kui vedelal heeliumil ja 3 korda suurem kui vedelal vesinikul.
Heeliumi kasutatakse tänu sellele lämmastiku asendamiseks hingavate gaaside komponendina vähene lahustuvus vedelikes, eriti lipiidides. Gaasid imenduvad verre ja kehakudedesse, kui on rõhk, näiteks sukeldumine, mis põhjustab anesteetilist toimet, mida nimetatakse sügavushaiguseks. Vähese lahustuvuse tõttu satub rakumembraanidesse vähe heeliumi, mis aitab vähendada narkootilist toimet.
Vähese põlengu ja kerguse tõttu ning pärast 1937. aasta Hindenburgi katastroofi asendas heelium kütuse tootmisel vesiniku, isegi hoolimata sellest, et ujuvus oli kadunud 8,6%
Neid gaase kasutatakse valgustuses nende juhtivuse tõttu. Hõõglampide valmistamisel kasutatakse nende täitmiseks argooni ja lämmastiku segu. Krüpton kasutatakse suure jõudlusega pirnidesnagu näiteks halogeenlambid, millel on kõrgem värvitemperatuur ja suurem efektiivsus.
Ksenooni kasutatakse tavaliselt ksenoonlaternates, mida päevavalgusega sarnase valgusspektri saavutades kasutatakse nii filmiprojektorites kui ka autode esilaternates.
Meditsiinis kasutatakse heeliumi astmahaigete hingamise hõlbustamiseks. Ksenooni saab kasutada anesteetikumina Tänu suurele lahustuvusele lipiidides, mis muudab selle efektiivsemaks kui tavaline dilämmastikoksiid, ja kuna organism on selle hõlpsasti elimineeritav, võimaldab see kiiremini taastuda.
Piltide hankimisel, mis viiakse läbi tuuma magnetresonantsi abil, on ksenoon ühendatud teiste gaasidega. Kiirgusteraapias kasutatakse radooni, mis on väga radioaktiivne ja saadaval ainult väheses koguses.
Tootmine ja arvukus
Väärisgaaside arvukus ja lihtsus on nende aatomite arvuga pöördvõrdelised. Seetõttu väheneb nende gaaside arvukus, kui nende aatomnumber suureneb.
Universumis, heelium on kõige lihtsam saada teine element, pärast vesinikku, massiprotsent on umbes 24%. Suurema osa heeliumi kogusest universumis moodustas ürgne nukleosüntees, kuid selle hulk suureneb tänu vesiniku osalemisele tähtede nukleosünteesis (protsess, mis tekib tuumareaktsioonidest tähtede evolutsiooniprotsessi käigus).
Ülejäänud gaase ei ole kaugeltki nii rikkalikult või lihtsalt saada. Radoon võib näiteks olla vormi litosfääris läbi raadiumi alfa lagunemise; Vahepeal ta ksenoon on välja töötanud teooria, mida nimetatakse "puuduva ksenooni teooriaks" selle suhteliselt väikese koguse tõttu atmosfääris.
Räägime kõigist natuke
- Helio: Tänu oma vähesele põlevusele ja kuna see on teine lihtsamini saadav element, on see suutnud vesiniku asendada potentsiaalse elemendina õhupallide ja tsepeliinide täitmiseks, kuna need ei plahvata tulega kokku puutudes.
- Neoon: Seda gaasi kasutatakse fluorestsentsi ja punase-oranži tooni tõttu, mis tekib kokkupuutel elektriga, reklaami eesmärgil. Kergesti neoonvalgustites. Samuti võite saada neoontorusid ja lampe, millel on muud värvid, kuigi tegelikult on nende sees muid gaase.
- Argoon: Seda gaasi kasutatakse hõõglampides, kuna see ei reageeri hõõgniidiga kõrge temperatuuri ja rõhu tingimustes. Luminofoorlampides tekitab see rohelise-sinise värvi. Seda kasutatakse ka tööstusvaldkonnas soovimatute keemiliste reaktsioonide vältimiseks.
- Krüpton: Seda kasutatakse koos muude gaasidega lampide loomisel ja valmistamisel lennujaama valgustus, tulenevalt eralduvate punaste tulede tugevusest; seda saab kasutada ka kinoprojektorites. Krüptooni kasutamine on kasulik ka võrkkesta laseroperatsioonides.
- Ksenoon: ksenooni peamine kasutusala on bakteritsiidsete omadustega valguse kiirgajate väljatöötamine; helendavad torud, fotovälgud ja ka rubiinlaseri ergastamise võimega luminofoorlambid.
- Radoon: See gaas tekib uraani radioaktiivsel lagunemisel raadioks. Seetõttu ja seetõttu, et see on väga radioaktiivne, on sellel igapäevases elus väga vähe rakendusi.
Mõtisklemiseks
Kuigi need on mõnevõrra kokku pandud looduslikus olekus on raske saada (välja arvatud võib-olla heelium) ja kuna need tekitavad või võimaldavad nendega üsna vähe reageerida, on väärisgaasid olulised ühendid, mida võime näha ja isegi igapäevaselt kasutada.
Võib-olla piirduvad nende kasutusalad konkreetsete valdkondadega, kuid see ei tähenda, et need oleksid täiesti kasutud. Alates kodu valgustamisest lambipirnides ja lampides kuni toidu säilitamiseni külmkapis kuni päästa meditsiinis kasutatuna inimelusidNeed looduslikud või sünteetilised gaasid pole veel näidanud kõike, mida nad saaksid meie heaks teha. Ja on kindel, et teadusuuringute edenedes on nende kasutamine palju suurem.
Mis on võime ioniseerida?
ja selle habras