Dentro de la química, existen infinidad de elementos que pueden estar relacionados o no entre sí. Están los metales, no metales, lantánidos y actínidos, metales de transición y alcalinotérreos; y, por supuesto, tenemos a unos de los elementos químicos a los que poca atención les hemos prestado durante las clases de química, y mucha menos a la hora de continuar con nuestras vidas. Hablo, claro está, de los gases nobles.
Estos elementos que, al ser tan poco frecuentes en el ambiente, no podemos analizar demasiado. Aquí conoceremos la historia de los gases nobles, sus usos y propiedades, así como también otras curiosidades. Quédate aquí y aprende las cosas más interesantes sobre los gases nobles.
Conozcamos los gases
Son un grupo de compuestos químicos con propiedades muy parecidas entre sí. Por ejemplo, bajo condiciones normales son gases incoloros, inodoros, monoatómicos, y presentan una reactividad química muy baja. Estos se sitúan en el grupo número 18 de la tabla periódica, y son conocidos como: Helio, neón, Xenón, Argón, Kriptón, el radioactivo: Radón, y el sintético: Oganesón.
Sus propiedades pueden ser explicadas por las teorías modernas existentes en la estructura atómica. A su capa de electrones valentes se las considera completas, lo cual les da una limitada tendencia a participar en reacciones químicas, y es una de las razones por las que son poco conocidos. De hecho, muy pocos compuestos con gases nobles han sido preparados hasta nuestros días.
¿De dónde sacamos los gases nobles?
El neón, argón, xenón y kriptón los obtenemos del aire al utilizar métodos de destilación fraccionada y licuefacción. El helio lo encontramos en el gas natural, de donde debe ser típicamente separado. Y el radón se obtiene a través del decaimiento radioactivo de compuestos disueltos en el radio.
Y el Oganesón es un elemento sintético creado en el 2002, y que obtuvo su nomenclatura IUPAC en el 2016. Se conoce por ser un elemento bastante reactivo a la par que inestable, por lo que no se ha trabajado mucho con él
Estos gases han tenido muy importantes utilidades en los campos de la iluminación, soldadura y exploración espacial. El trimix, que es una disolución de helio-oxígeno-nitrógeno, se emplea en para que los buzos no sufran el efecto narcótico del nitrógeno en las profundidades. Además, luego de conocerse los riesgos de inflamabilidad del hidrógeno, este fue reemplazado por helio en la creación de dirigibles y globos aerostáticos.
Propiedades de estos gases
Los gases nobles deben su nombre a la traducción del alemán Edelgas, nombre utilizado por primera vez en 1898 por el químico Hugo Erdman. Con este nombre buscaba referirse a la baja tasa de reactividad de estos elementos. De hecho, estos son los elementos menos reactivos que se conocen, tanto así que son prácticamente inertes o no-reactivos.
Esto se debe a que cuentan con una capa de valencia completa lo cual les deja una baja capacidad para liberar electrones y hace que su comportamiento se encuentre cerca del de un gas ideal.
En general, los gases nobles comparten distintas propiedades.
- Son elementos no metálicos: al ser gases, no tiene partícula alguna de metal dentro de su conformación. Al mismo tiempo no son capaces de reaccionar con otros metales.
- No tienen color ni olor: a pesar de que pueden dársele colores a los bombillos y lámparas creadas por medio de estos gases utilizando la electricidad, ellos originalmente no tienen color, y son inodoros.
- Tienen una capa de valencia completa: El neón el xenón, el argón, el kriptón y el radón presentan ocho electrones en su última capa. Por su parte, el helio tiene dos electrones. De esta forma, los gases nobles tienen una capa de valencia completa. Es por ello que, en circunstancias normales, estos elementos no forman enlaces
- Existen como gases monoatómicos: Como se entiende, estos elementos, incluso el más grande atómicamente, solo presentan un átomo.
- Son prácticamente no reactivos: Debido a su valencia completa y su dificultad para entregar electrones, se les considera como prácticamente inertes.
- Conducen electricidad y producen fluorescencia: Aunque de manera muy baja, estos gases son capaces de conducir electricidad, y al hacerlo brillan con fosforescencia.
- Tienen una baja temperatura de fusión y de ebullición: estos gases nobles presentas puntos tanto de fusión como de ebullición realmente bajos.
- Poseen una electronegatividad muy baja: estos elementos son muy poco electronegativos
- Tienen una alta energía de ionización: Su energía de ionización es en realidad la más alta en su período.
- No son inflamables: Incluso debido a la taza inflamable del hidrógeno, fue reemplazado por el helio en la fabricación de dirigibles y globos.
Al igual que ocurre con la reactividad, sus fuerzas interatómicas también son muy débiles, por lo cual tienen unas bajas temperaturas de fusión y de ebullición, y todos son gases monoatómicos en condiciones normales, incluyendo a los gases de mayor masa atómica.
El helio posee muchas propiedades que no tiene ningún otro gas noble ni ningún otro elemento de la tabla periódica. Su punto de fusión es el más bajo en todos los conocidos, además de ser el único elemento dueño de un estado de superfluidez; un estado en el que la materia está en estado líquido, pero que puede correr sin perder energía cinética. El helio necesita una presión de 25atm y una temperatura de -272ºC para poder solidificar.
Su capa de valencia completa también es responsable de que estos gases tengan una gran capacidad de ionización (la más alta de la tabla periódica) y no pueden formar iones fácilmente, lo cual demuestra su estabilidad en su configuración electrónica.
La energía de ionización va decreciendo a la misma medida que se decrece de grupo, pues aumenta el radio atómico y los electrones de valencia están más lejos del núcleo y por lo tanto menos atraídos hacia él. Esto causa que, aunque en su periodo sea la más alta, algunos gases nobles tienen una energía de ionización comparable a la de otros elementos. Por ejemplo, la energía de ionización del xenón es comparable con la energía de ionización del oxígeno.
Usos de estos gases
Al tener puntos de ebullición y fusión tan bajos, son especialmente útiles en la elaboración de equipos de refrigeración, y los hace útiles también como refrigerantes criogénicos.
El helio líquido, que hierve a 4,2K (-268,93ºC) es utilizado en la fabricación de imanes superconductores, como los utilizados para la imagen por resonancia magnética, y la resonancia magnética nuclear.
El neón líquido, si bien no llega a las bajas temperaturas del helio líquido, tiene más aplicaciones en la criogenia, pues tiene una capacidad de refrigeración 40 veces mayor que la de el helio líquido y 3 veces mayor que la del hidrógeno líquido.
El helio se utiliza como componente de los gases respirables para sustituir al nitrógeno, gracias a su baja solubilidad en fluidos, especialmente en los lípidos. Los gases son absorbidos por la sangre y los tejidos corporales cuando hay presión, como el submarinismo, lo que produce un efecto anestésico llamado mal de profundidad. Debido a su baja solubilidad, entra poco helio a las membranas celulares, lo cual ayuda a frenar el efecto narcótico.
Debido a su poca combustibilidad y su ligereza, y tras el desastre del Hindenburg de 1937, el helio sustituyó al hidrógeno en la fabricación de combustible, aún pese a una pérdida de flotabilidad del 8,6%
Estos gases se utilizan en la iluminación debido a su conductividad. En la fabricación de bombillas incandescentes se utiliza una mezcla de argón y nitrógeno para rellenarlas. El kriptón se usa en bombillas de alto rendimiento, como las lámparas de halógeno, que tienen una temperatura de color más elevada y una mayor eficacia.
El xenón es comúnmente usado en faros de xenón, que, al lograr un espectro de luz parecido a la luz del día es utilizado en proyectores de películas así como en faros de automóvil.
En la medicina, el helio es utilizado para mejorar la facilidad de respiración de los pacientes con asma. El xenón puede utilizarse como un anestésico debido a su alta solubilidad en lípidos, lo cual lo hace más eficaz que el habitual óxido nitroso, y como es eliminado fácilmente por el cuerpo, permite un restablecimiento más rápido.
La captación de imágenes que se lleva a cabo por medio de resonancia magnética nuclear, tiene al xenón combinado con otros gases. El radón, que es muy radiactivo y solo está disponible en mínimas cantidades se utiliza en el tratamiento por radioterapia.
Producción y abundancia
La abundancia y facilidad con la que los gases nobles pueden conseguirse están en inversa proporción a su número atómico. Por lo tanto, la abundancia de estos gases disminuye conforme aumenta su número atómico.
En el universo, el helio es el segundo elemento que más fácil puede conseguirse, después del hidrógeno, con un porcentaje de masa de aproximadamente el 24%. La mayoría de la cantidad de helio en el universo se formó mediante la nucleosíntesis primordial, pero su cantidad va en aumento gracias a la participación del hidrógeno en la nucleosíntesis estelar (proceso que surge por reacciones nucleares durante el proceso evolutivo de las estrellas).
El resto de los gases no son ni de lejos tan abundantes ni simples de conseguir. El radón, por ejemplo, se puede formar en la litosfera a través de la desintegración alfa del radio; mientras que el xenón ha desarrollado una teoría conocida como “teoría del xenón desaparecido” debido a su cantidad relativamente baja en la atmósfera.
Hablemos un poco de cada uno
- Helio: Por su poca combustibilidad, y por ser el segundo elemento más fácil de conseguir, ha podido reemplazar al hidrógeno como el elemento en potencia para llenar globos y zepelines, pues estos no estallan al ponerse en contacto con fuego
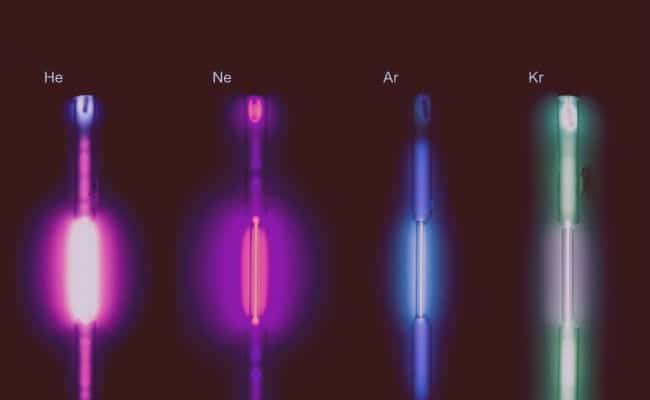
- Neón: Este gas, debido a su fluorescencia y a su tonalidad rojo-anaranjado obtenida cuando se pone en contacto con electricidad es utilizado con fines publicitarios, encontrados más fácilmente en las luces de neón. También se consiguen tubos y lámparas de neón que tienen otros colores, aunque en realidad tienen dentro otros gases.
- Argón: Este gas se emplea en lámparas incandescentes porque no reacciona con el filamento en altas condiciones de temperatura y presión. En tubos fluorescentes genera un color verde-azul. También se utiliza en el campo industrial para evitar reacciones químicas no deseadas.
- Kriptón: Se utiliza junto con otros gases en la creación y elaboración de lámparas de iluminación de aeropuertos, debido a la intensidad de las luces rojas emitidas; también puede usarse en proyectores de cine. El uso del kriptón es también útil en la cirugía de retina con láser.
- Xenón: el uso principal del Xenón es la elaboración de emisores de luz con características bactericidas; tubos luminosos, flashes fotográficos, y también en tubos fluorescentes con capacidad de excitar el láser de rubí.
- Radón: Este gas se genera por la desintegración radiactiva del uranio a radio. Por esto y porque resulta muy radiactivo posee muy pocas aplicaciones en la vida diaria.
Para reflexionar
A pesar de que sean compuestos un tanto difíciles de conseguir en estado natural (excepto, quizás por el helio), y por el hecho de que generan o se permiten más bien pocas reacciones con ellos, los gases nobles son compuestos importantes que podemos ver, e incluso utilizar diariamente.
Quizás sus usos estén limitados a campos específicos, pero eso no quiere decir que sean del todo inútiles. Desde iluminar nuestros hogares en bombillas y lámparas, pasando por mantener nuestros alimentos al utilizarse en refrigeradores, hasta salvar vidas cuando se usan en la medicina, estos gases, naturales o sintéticos, no han demostrado todavía todo lo que pueden hacer por nosotros. Y es seguro que, a medida que vayan avanzando las investigaciones, su uso será mucho mayor.
CUal es la capacidad para ionizarse?
y su fragilidad