રસાયણશાસ્ત્રમાં, ત્યાં અસંખ્ય તત્વો હોય છે જે એક બીજાથી સંબંધિત હોઈ શકે છે અથવા ન પણ હોય છે. ત્યાં ધાતુઓ, નોનમેટલ્સ, લેન્ટિનાઇડ્સ અને એક્ટિનાઇડ્સ, સંક્રમણ ધાતુઓ અને આલ્કલાઇન પૃથ્વી છે; અને અલબત્ત અમારી પાસે છે એક રાસાયણિક તત્વો છે જેની તરફ આપણે રસાયણશાસ્ત્રના વર્ગો દરમિયાન થોડું ધ્યાન આપ્યું છે, અને જ્યારે આપણા જીવન સાથે આગળ વધવાની વાત આવે છે ત્યારે ઘણું ઓછું હોય છે. હું અલબત્ત, ઉમદા વાયુઓ વિશે બોલું છું.
આ તત્વો કે જે પર્યાવરણમાં ખૂબ ઓછા હોવાને કારણે આપણે વધારે વિશ્લેષણ કરી શકતા નથી. અહીં આપણે ઉમદા વાયુઓના ઇતિહાસ, તેમના ઉપયોગ અને ગુણધર્મો, તેમજ અન્ય જિજ્ .ાસાઓ વિશે શીખીશું. અહીં રહો અને ઉમદા વાયુઓ વિશે શાનદાર વસ્તુઓ શીખો.
ચાલો વાયુઓ જાણીએ
તે રાસાયણિક સંયોજનોનું એક જૂથ છે જે એકબીજા સાથે સમાન ગુણધર્મો ધરાવે છે. ઉદાહરણ તરીકે, સામાન્ય સ્થિતિમાં તે રંગહીન, ગંધહીન, એકવાસ્તિક વાયુઓ હોય છે અને રાસાયણિક પ્રતિક્રિયા ખૂબ ઓછી હોય છે. આ સામયિક કોષ્ટકના જૂથ નંબર 18 માં સ્થિત છે, અને આના નામથી ઓળખાય છે: હેલિયમ, નિયોન, ઝેનોન, આર્ગન, ક્રિપ્ટોન, કિરણોત્સર્ગી: રેડોન અને કૃત્રિમ: ઓગનેસન.
તેના ગુણધર્મોને અણુ માળખું પરના હાલના આધુનિક સિદ્ધાંતો દ્વારા સમજાવી શકાય છે. તેમના વેલેન્ટ ઇલેક્ટ્રોનના શેલને સંપૂર્ણ માનવામાં આવે છે, જે તેમને રાસાયણિક પ્રતિક્રિયાઓમાં ભાગ લેવાનું મર્યાદિત વલણ આપે છે, અને તે નબળા સમજવા માટેનું એક કારણ છે. હકીકતમાં, આજ સુધી ખૂબ જ ઓછા ઉમદા ગેસ સંયોજનો તૈયાર કરવામાં આવ્યા છે.
આપણને ઉમદા વાયુઓ ક્યાંથી મળે છે?
અપૂર્ણાંક નિસ્યંદન અને લિક્વિફેક્શન પદ્ધતિઓનો ઉપયોગ કરીને આપણે હવામાં નિયોન, આર્ગોન, ઝેનોન અને ક્રિપ્ટન મેળવીએ છીએ. હેલિયમ કુદરતી ગેસમાં જોવા મળે છે, જ્યાં તે સામાન્ય રીતે અલગ થવું જોઈએ. અને રેડન રેડિયમમાં ઓગળેલા સંયોજનોના કિરણોત્સર્ગી સડો દ્વારા પ્રાપ્ત થાય છે.
અને ઓગાનેસન એ એક કૃત્રિમ તત્ત્વ છે જેનું નિર્માણ 2002 માં કરવામાં આવ્યું હતું, અને જેણે તેનું આઇયુપીએસી નામકરણ 2016 માં મેળવ્યું હતું. તે એકદમ પ્રતિક્રિયાશીલ તેમજ અસ્થિર હોવા માટે જાણીતું છે, તેથી તેની સાથે વધારે કામ કરવામાં આવ્યું નથી.
આ વાયુઓના લાઇટિંગ, વેલ્ડીંગ અને અવકાશ સંશોધન ક્ષેત્રે ખૂબ જ મહત્વપૂર્ણ ઉપયોગો થયા છે. ટ્રિમિક્સ, જે હિલીયમ-oxygenક્સિજન-નાઇટ્રોજનનો ઉકેલો છે, તેનો ઉપયોગ થાય છે જેથી ડાઇવર્સ theંડાણોમાં નાઇટ્રોજનના માદક અસરનો ભોગ ન બને. બીજું શું છે, હાઇડ્રોજનના જ્વલનશીલતા જોખમોને જાણ્યા પછી, આને એરિશીપ્સ અને હોટ એર ફુગ્ગાઓના નિર્માણમાં હિલીયમ દ્વારા બદલવામાં આવ્યું હતું.
આ વાયુઓના ગુણધર્મો
ઉમદા વાયુઓ જર્મનના અનુવાદમાંથી તેમનું નામ મેળવે છે એડેલગાસ, નામ રસાયણશાસ્ત્રી હ્યુગો એર્ડમેન દ્વારા 1898 માં પ્રથમ વખત ઉપયોગમાં લેવાયો હતો. આ નામ સાથે નીચા પ્રતિક્રિયાશીલતા દરનો સંદર્ભ લેવાની માંગ કરી આ તત્વો છે. હકીકતમાં, આ જાણીતા ઓછામાં ઓછા પ્રતિક્રિયાશીલ તત્વો છે, એટલા બધા કે તેઓ વ્યવહારીક નિષ્ક્રિય અથવા બિન-પ્રતિક્રિયાશીલ છે.
આ કારણ છે કે તેમની પાસે સંપૂર્ણ વેલેન્સ શેલ છે જે તેમને ઇલેક્ટ્રોનને મુક્ત કરવાની ઓછી ક્ષમતા સાથે છોડી દે છે અને તેમના વર્તનને આદર્શ ગેસની નજીક બનાવે છે.
સામાન્ય રીતે, ઉમદા વાયુઓ વિવિધ ગુણધર્મો વહેંચે છે.
- તેઓ બિન-ધાતુ તત્વો છે: વાયુઓ હોવાને કારણે તેની રચનામાં ધાતુનો કણો હોતો નથી. તે જ સમયે તેઓ અન્ય ધાતુઓ સાથે પ્રતિક્રિયા આપવા માટે સક્ષમ નથી.
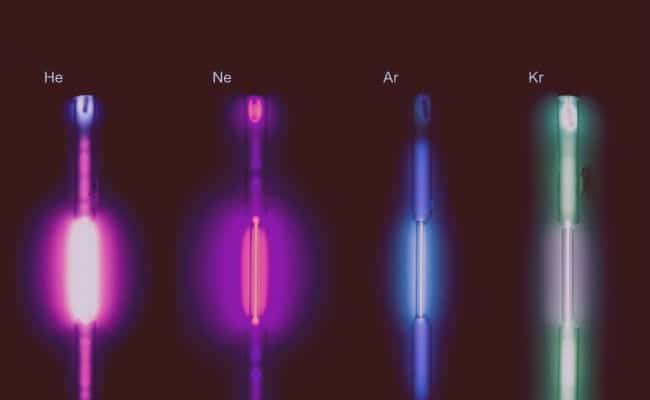
- તેઓ રંગહીન અને ગંધહીન છે: જોકે તેઓ આપી શકાય છે બલ્બ અને લેમ્પ્સ માટે રંગો વીજળીનો ઉપયોગ કરીને આ વાયુઓ દ્વારા બનાવવામાં આવેલ છે, તે મૂળ રંગહીન અને ગંધહીન છે.
- તેમની પાસે સંપૂર્ણ વેલેન્સ સ્તર છે: નિયોન, ઝેનોન, આર્ગોન, ક્રિપ્ટોન અને રેડોનના છેલ્લા શેલમાં આઠ ઇલેક્ટ્રોન છે. તેના ભાગ માટે, હિલીયમ પાસે બે ઇલેક્ટ્રોન છે. આ રીતે, ઉમદા વાયુઓમાં સંપૂર્ણ વેલેન્સ શેલ હોય છે. તેથી જ, સામાન્ય સંજોગોમાં, આ તત્વો કડીઓ બનાવતા નથી.
- તેઓ મોનોટોમિક વાયુઓ તરીકે અસ્તિત્વ ધરાવે છે: સમજ્યા મુજબ, આ તત્વો, સૌથી મોટા પરમાણુ પણ, ફક્ત એક જ અણુ ધરાવે છે.
- તેઓ વ્યવહારીક બિન-પ્રતિક્રિયાશીલ છે: તેમની સંપૂર્ણ તંદુરસ્તી અને ઇલેક્ટ્રોન પહોંચાડવામાં તેમની મુશ્કેલીને કારણે, તેઓ વ્યવહારીક નિષ્ક્રિય માનવામાં આવે છે.
- તેઓ વીજળી ચલાવે છે અને ફ્લોરોસન્સ ઉત્પન્ન કરે છેખૂબ ઓછી હોવા છતાં, આ વાયુઓ વીજળી ચલાવવામાં સક્ષમ છે, અને આમ કરવામાં તેઓ ફોસ્ફોરેસન્ટલી ગ્લો કરે છે.
- તેમની પાસે ગલન અને ઉકળતા બિંદુઓ ઓછા છેઆ ઉમદા વાયુઓ ખૂબ જ ઓછી ગલન અને ઉકળતા બિંદુઓ ધરાવે છે.
- તેમની પાસે ખૂબ ઓછી ઇલેક્ટ્રોનેક્ટીવીટી છે: આ તત્વો ખૂબ ઓછા ઇલેક્ટ્રોનેગેટિવ હોય છે
- તેમની પાસે ઉચ્ચ આયનીકરણ energyર્જા છે: તમારી આયનાઇઝેશન energyર્જા ખરેખર તમારા સમયગાળામાં સૌથી વધુ છે.
- તેઓ જ્વલનશીલ નથી: હાઈડ્રોજનના જ્વલનશીલ કપને લીધે પણ, એરિશીપ્સ અને ફુગ્ગાઓના ઉત્પાદનમાં હિલીયમ દ્વારા તેનું સ્થાન લેવામાં આવ્યું.
પ્રતિક્રિયાશીલતાની જેમ, તેમની આંતરસંબંધીય શક્તિઓ પણ ખૂબ નબળી છે, તેથી જ તેમની પાસે ગલન અને ઉકળતા તાપમાન ઓછા છે, અને તે બધા સામાન્ય સ્થિતિઓ હેઠળ એક્યુટોમિક વાયુઓ છે, જેમાં ઉચ્ચ અણુ સમૂહવાળા વાયુઓનો સમાવેશ થાય છે.
હિલીયમમાં ઘણી ગુણધર્મો છે જે સામયિક ટેબલ પર કોઈ અન્ય ઉમદા ગેસ અથવા અન્ય કોઈ તત્વ પાસે નથી. તેના ગલનબિંદુ સૌથી નીચો છે બધા જાણીતા લોકોમાં, અતિશય પ્રવાહની સ્થિતિ ધરાવતા એકમાત્ર તત્વ હોવા ઉપરાંત; એક રાજ્ય જેમાં દ્રવ્ય પ્રવાહી સ્થિતિમાં છે, પરંતુ ગતિશક્તિ ગુમાવ્યા વિના ચાલી શકે છે. હેલિયમને મજબૂત બનાવવા માટે 25atm નું દબાણ અને -272 -C તાપમાનની જરૂર છે.
તેમનો સંપૂર્ણ વેલેન્સ શેલ પણ આ વાયુઓ માટે ઉચ્ચ આયનીકરણ ક્ષમતા (સમયાંતરે કોષ્ટકમાં સૌથી વધુ) માટે જવાબદાર છે. અને આયનો સરળતાથી બનાવી શકતા નથીછે, જે તેના ઇલેક્ટ્રોનિક ગોઠવણીમાં તેની સ્થિરતા દર્શાવે છે.
જૂથમાં ઘટાડો થતાં આયનીકરણ energyર્જામાં ઘટાડો થાય છે, કારણ કે અણુ ત્રિજ્યા વધે છે અને વેલેન્સ ઇલેક્ટ્રોન બીજકથી વધુ દૂર હોય છે અને તેથી તેના તરફ ઓછું આકર્ષિત થાય છે. આ કારણોસર છે, તેમનો સમયગાળો સૌથી વધુ હોવા છતાં, કેટલાક ઉમદા વાયુઓ ધરાવે છે તુલનાત્મક આયનીકરણ energyર્જા અન્ય તત્વો છે કે. ઉદાહરણ તરીકે, ઝેનોનની આયનીકરણ energyર્જા oxygenક્સિજનની આયનીકરણ energyર્જા સાથે તુલનાત્મક છે.
આ વાયુઓના ઉપયોગ
આવા ઉકળતા અને ગલનબિંદુઓ ઓછા હોવાને કારણે, તેઓ ખાસ કરીને રેફ્રિજરેશન સાધનોના ઉત્પાદનમાં ઉપયોગી છે, અને તેમને ક્રાયોજેનિક રેફ્રિજરેન્ટ્સ તરીકે પણ ઉપયોગી બનાવે છે.
લિક્વિડ હિલિયમ, જે 4,2K (-268,93C) પર ઉકળે છે તેનો ઉપયોગ સુપરકંડક્ટિંગ ચુંબકના ઉત્પાદનમાં થાય છે, જેમ કે મેગ્નેટિક રેઝોનન્સ ઇમેજિંગ અને અણુ મેગ્નેટિક રેઝોનન્સ માટે વપરાય છે.
લિક્વિડ નિયોન, જોકે તે પ્રવાહી હિલીયમના નીચા તાપમાને પહોંચતું નથી, ક્રિઓજેનિક્સમાં વધુ એપ્લિકેશન ધરાવે છે, કારણ કે તેની ક્ષમતા છે પ્રવાહી હિલીયમ કરતાં 40 ગણા વધુ ઠંડક અને પ્રવાહી હાઇડ્રોજન કરતા 3 ગણો વધારે છે.
નાઇટ્રોજનને બદલવા માટે, શ્વાસનીય વાયુઓના ઘટક તરીકે હેલિયમનો ઉપયોગ થાય છે, આભાર પ્રવાહીમાં ઓછી દ્રાવ્યતાખાસ કરીને લિપિડ્સમાં. જ્યારે દબાણ હોય ત્યારે વાયુ લોહી અને શરીરના પેશીઓમાં સમાઈ જાય છે, જેમ કે સ્કુબા ડાઇવિંગ, જે એનેસ્થેટિક અસર પેદા કરે છે જેને ડેપ્થ બીમારી કહેવાય છે. તેની ઓછી દ્રાવ્યતાને લીધે, થોડું હિલીયમ સેલ પટલમાં પ્રવેશ કરે છે, જે માદક અસરને કાબૂમાં કરવામાં મદદ કરે છે.
તેની ઓછી જ્વલનશીલતા અને હળવાશને કારણે અને 1937 ની હિંદનબર્ગ વિનાશ પછી, હિલીયમે બળતણના ઉત્પાદનમાં હાઇડ્રોજનને બદલ્યું, 8,6% ની ઉમંગની ખોટ છતાં પણ
આ વાયુઓ તેમની વાહકતાને કારણે લાઇટિંગમાં ઉપયોગમાં લેવાય છે. અગ્નિથી પ્રકાશિત બલ્બના નિર્માણમાં આર્ગોન અને નાઇટ્રોજનનું મિશ્રણ તેમને ભરવા માટે થાય છે. ક્રિપ્ટોન ઉચ્ચ પ્રભાવ બલ્બ વપરાય છેજેમ કે હેલોજન લેમ્પ્સ, જેનો રંગ temperatureંચો તાપમાન અને efficંચી અસરકારકતા ધરાવે છે.
ઝેનોનનો ઉપયોગ સામાન્ય રીતે ઝેનોન હેડલાઇટમાં થાય છે, જે, દિવસના પ્રકાશ જેવા સમાન લાઇટ સ્પેક્ટ્રમ પ્રાપ્ત કરીને, ફિલ્મ પ્રોજેક્ટર તેમજ કાર હેડલાઇટમાં વપરાય છે.
દવામાં દર્દીઓમાં હિલીયમ શ્વાસની સરળતામાં સુધારો કરવા માટે વપરાય છે. ઝેનોન એનેસ્થેટિક તરીકે વાપરી શકાય છે લિપિડ્સમાં તેની solંચી દ્રાવ્યતાને કારણે, જે તેને સામાન્ય નાઇટ્રસ oxકસાઈડ કરતાં વધુ અસરકારક બનાવે છે, અને શરીર દ્વારા તે સરળતાથી દૂર થઈ જાય છે, તેથી તે ઝડપી પુન recoveryપ્રાપ્તિને મંજૂરી આપે છે.
પરમાણુ ચુંબકીય પડઘો માધ્યમ દ્વારા હાથ ધરવામાં આવતી છબીઓનું કેપ્ચર, અન્ય વાયુઓ સાથે ઝેનોન સાથે જોડાયેલું છે. રેડન, જે ખૂબ કિરણોત્સર્ગી છે અને તે ફક્ત ટ્રેસ પ્રમાણમાં ઉપલબ્ધ છે, તેનો ઉપયોગ કિરણોત્સર્ગ ઉપચારની સારવારમાં થાય છે.
ઉત્પાદન અને વિપુલતા
ઉમદા વાયુઓ મેળવી શકાય તેટલી વિપુલતા અને સરળતા તેમની અણુ સંખ્યાના વિપરિત પ્રમાણમાં છે. તેથી, આ વાયુઓની વિપુલતામાં ઘટાડો થાય છે કારણ કે તેમની અણુ સંખ્યામાં વધારો થાય છે.
બ્રહ્માંડમાં, હિલીયમ મેળવવાનું બીજું સૌથી સરળ તત્વ છે, હાઇડ્રોજન પછી, આશરે 24% ની સામૂહિક ટકાવારી. બ્રહ્માંડમાં હિલીયમનો મોટાભાગનો જથ્થો પ્રાચીન ન્યુક્લિયોસિંથેસિસ દ્વારા બનાવવામાં આવ્યો હતો, પરંતુ તારાઓની ન્યુક્લિયોસિંથેસિસ (તારાઓની ઉત્ક્રાંતિ પ્રક્રિયા દરમિયાન પરમાણુ પ્રતિક્રિયાઓ દ્વારા ઉદ્ભવતા પ્રક્રિયા) માં હાઇડ્રોજનની ભાગીદારીને કારણે તેની માત્રા વધારી રહી છે.
બાકીના વાયુઓ જેટલા વિપુલ પ્રમાણમાં અથવા પ્રાપ્ત કરવા જેટલા સરળ નથી. રેડોન, ઉદાહરણ તરીકે, હોઈ શકે છે લિથોસ્ફીયરમાં રચાય છે રેડિયમના આલ્ફા સડો દ્વારા; દરમિયાન તેમણે ઝેનોને એક સિદ્ધાંત વિકસાવી છે જેને "ગુમ થયેલ ઝેનોન થિયરી" તરીકે ઓળખવામાં આવે છે. વાતાવરણમાં તેની પ્રમાણમાં ઓછી માત્રાને કારણે.
ચાલો દરેક વિશે થોડી વાત કરીએ
- Helio: તેની ઓછી જ્વલનશીલતાને લીધે, અને તે મેળવવા માટેનું બીજું સૌથી સરળ તત્વ હોવાથી, તે ફુગ્ગાઓ અને ઝેપ્લીન ભરવા માટેના સંભવિત તત્વ તરીકે હાઇડ્રોજનને બદલવામાં સક્ષમ છે, કારણ કે જ્યારે તેઓ આગના સંપર્કમાં આવે છે ત્યારે તે ફૂટતા નથી.
- નિયોન: આ ગેસ, તેના ફ્લોરોસન્સ અને તેના લાલ-નારંગી રંગને કારણે જ્યારે તે વીજળીના સંપર્કમાં આવે છે, તેનો ઉપયોગ જાહેરાત હેતુ માટે થાય છે. નિયોન લાઇટમાં સરળતાથી મળી. તમે નિયોન ટ્યુબ અને લેમ્પ્સ પણ મેળવી શકો છો જેમાં અન્ય રંગો છે, જો કે તેમાં ખરેખર અન્ય વાયુઓ હોય છે.
- આર્ગોન: આ ગેસનો ઉપયોગ અગ્નિથી પ્રકાશિત દીવાઓમાં થાય છે કારણ કે તે તાપમાન અને દબાણની conditionsંચી પરિસ્થિતિઓમાં ફિલામેન્ટ સાથે પ્રતિક્રિયા આપતું નથી. ફ્લોરોસન્ટ ટ્યુબમાં તે લીલો-વાદળી રંગ પેદા કરે છે. અનિચ્છનીય રાસાયણિક પ્રતિક્રિયાઓ ટાળવા માટે તેનો ઉપયોગ industrialદ્યોગિક ક્ષેત્રમાં પણ થાય છે.
- ક્રિપ્ટોન: તેનો ઉપયોગ લેમ્પ્સના નિર્માણ અને નિર્માણમાં અન્ય વાયુઓ સાથે મળીને થાય છે એરપોર્ટ લાઇટિંગ, રેડ લાઇટ્સની તીવ્રતાને કારણે; તેનો ઉપયોગ સિનેમા પ્રોજેક્ટરમાં પણ થઈ શકે છે. ક્રિપ્ટનનો ઉપયોગ લેસર રેટિના સર્જરીમાં પણ ઉપયોગી છે.
- ઝેનોન: ઝેનોનનો મુખ્ય ઉપયોગ બેક્ટેરિયાનાશક લાક્ષણિકતાઓવાળા પ્રકાશ ઉત્સર્જકોનું વિસ્તરણ છે; લ્યુમિનસ ટ્યુબ, ફોટોગ્રાફિક ચમકતા અને રૂબી લેસરને ઉત્તેજિત કરવાની ક્ષમતાવાળા ફ્લોરોસન્ટ ટ્યુબમાં પણ.
- રેડોન: આ ગેસ રેડિયોથી યુરેનિયમના કિરણોત્સર્ગી સડો દ્વારા ઉત્પન્ન થાય છે. આને કારણે અને કારણ કે તે ખૂબ કિરણોત્સર્ગી છે, તેના દૈનિક જીવનમાં ખૂબ ઓછા કાર્યક્રમો છે.
વિચારવું
તેમ છતાં તેઓ કંઈક અંશે રચાયેલ છે પ્રાકૃતિક સ્થિતિમાં પ્રાપ્ત કરવું મુશ્કેલ (કદાચ હિલીયમ સિવાય), અને કારણ કે તેઓ તેમની સાથે થોડા પ્રતિક્રિયા પેદા કરે છે અથવા મંજૂરી આપે છે, ઉમદા વાયુઓ એ મહત્વપૂર્ણ સંયોજનો છે જે આપણે જોઈ શકીએ છીએ, અને તે પણ દૈનિક ધોરણે ઉપયોગમાં લઈએ છીએ.
કદાચ તેમના ઉપયોગો ચોક્કસ ક્ષેત્રો સુધી મર્યાદિત છે, પરંતુ તેનો અર્થ એ નથી કે તે સંપૂર્ણપણે નકામું છે. અમારા ઘરોને લાઇટ બલ્બ અને લેમ્પ્સમાં પ્રગટાવવાથી લઈને, રેફ્રિજરેટરમાં ઉપયોગમાં લેવામાં આવે ત્યારે અમારા ખોરાકને રાખવા માટે જ્યારે દવામાં વપરાય છે ત્યારે જીવ બચાવોઆ વાયુઓ, કુદરતી અથવા કૃત્રિમ, હજી સુધી તે આપણા માટે જે કરી શકે તે બતાવી નથી. અને તે નિશ્ચિત છે કે જેમ જેમ સંશોધન પ્રગતિ કરે છે તેમ તેમ તેનો ઉપયોગ વધારે થશે.
આયનોઇઝ કરવાની ક્ષમતા શું છે?
અને તેની નાજુકતા