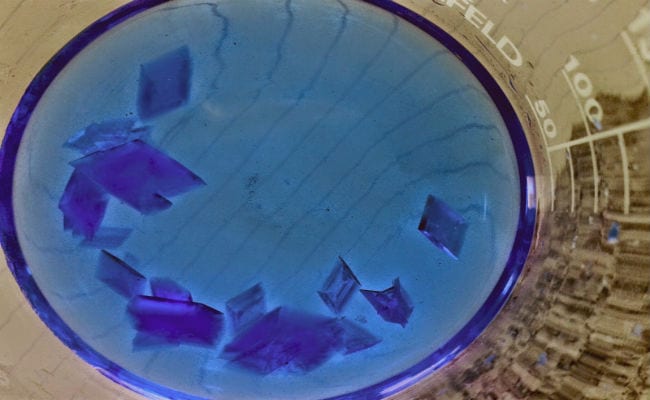
Sikkert at du noen gang har hørt om krystaller, er det sannsynlig at tankene dine på dette tidspunktet har visualisert en stor diamant, en ametyst eller en topas. Og absolutt, denne gruppen inkluderer også mange av de kjente "Dyrebare steiner", men en krystall er ikke en betegnelse som tydelig omfatter smykkefeltet.
En krystall er sluttproduktet av en interessant prosess kjent som krystallisering, som er preget av å resultere i et homogent fast stoff dannet av "ansikter", som er deler plassert i forskjellige plan.
Kjennetegn ved faststoff fra krystallisering
Størrelsen på en krystall er en variabel karakteristikk, i et bredt spekter av dimensjoner. "Enorme" krystaller kan bli funnet som kan måles gjennom den lineære enheten "meter", så godt vi kan finn krystaller det må være uttrykt som "mikron", siden deres lille størrelse gjør dem sammenlignbare med mikroorganismer som bakterier, som bare kan observeres gjennom mikroskopet.
Som nevnt resulterer krystallinske prosesser i produkter med høy renhet, det er derfor vi tidligere i definisjonen etablerte det krystallene er homogene: det vil si at sammensetningen av produktet forblir på en konstant verdi når som helst i volumet av det faste stoffet, noe som også innebærer at de fysiske og kjemiske egenskapene forblir uendret i hele stykket, og i tilfelle variasjon observeres på grunn av en forstyrrelse, endringen vil skje i hele arten. Denne kvaliteten gjør krystaller til verdifulle produkter innen forskjellige felt, alt fra verdsettelse av materialets kvalitet til bruk av krystalliseringsprosessen som en teknikk for å skille stoffer.
Krystallinske produkter kan også isoleres på laboratorienivå gjennom kontrollerte reaksjoner i samlinger som etterligner de spontane prosessene som oppstår i naturen. En av de viktigste fordelene med krystallene som oppnås i kontrollerte prosesser, er at de presenterer mer regelmessige former, som passer perfekt til de polygonale figurene med større nøyaktighet.
I en krystall må vi skille ansiktene som er en del av den virkelige krystallinske vanen (morfologiske egenskaper), og basert på antall av dem, kan vi vurdere grunnleggende former for det faste stoffet. Vanligvis i en krystall er definert av kombinasjonen av flere grunnleggende formerde viktigste er følgende:
- Pedion: Glass som består av et enkelt flatt ansikt, uten ekvivalenter.
- Pinacoid: Den består av to ekvivalente ansikter i forhold til en symmetriakse.
- Sphenoid: De to ekvivalente ansiktene som utgjør dette solide ligger rundt en binær akse.
- Prisme: Den består av homologe ansikter som utgjør en sone. Å være "krystallområdet" definert som et sett med ansikter parallelt med samme retning, tilsvarende en kant av den samme.
Strukturen til krystaller fra et internt synspunkt kan betraktes som utgjort av et mer eller mindre homogent, periodisk og anisotropisk system av et oppløst materiale som utvikler en struktur på forskjellige steder i rommet. Innenfor egenskapene til krystallene har interesse alltid blitt vekket av det faktum at hvert punkt gjenta regelmessig i rommet okkupert av materialet. I krystallografi kalles fenomenet som påvirker denne handlingen oversettelse.
Krystalliseringsprosess
For at krystallisering skal skje, må vi starte fra et stoff som kan klassifiseres som "Krystallinsk", og dette er definert fordi partiklene som utgjør det, enten de er av atomær, molekylær eller ionisk natur, har egenskaper av homogenitet, periodisitet og symmetri.
Hele prosessen aktiveres når partiklene begynner å omorganisere seg på et tidspunkt i det krystallinske stoffet, i et stadium kjent som nukleering. Hele denne prosessen involverer, i tillegg til den tydelige variasjonen i rekkefølgen av partiklene, en prosess med endring i de termodynamiske forholdene, som er orientert mot kompensasjonen av forstyrrelsene som genereres av endringen i Gibbs fri energi, som er preget av tre arrangementer:
- Endringen i kjemisk energi.
- Opprettelsen av et grensesnitt mellom kimdannelsessonen og resten av den homogene fasen.
- Variasjonen i volum og form som denne prosessen innebærer, utløser spenninger.
Den neste fasen har sin opprinnelse når kjernebasestrukturen stabiliseres. Det neste trinnet er noe logisk og forutsigbart, når vi har den grunnleggende strukturen, vil vi gå inn i en prosess med vekst, hvor en endring i dimensjonene til kjernen observeres. Litt etter litt vil denne økningen resultere i dannelse av ansikter, til krystallet tilegner seg en veldefinert vane.
Mekanisme for krystallvekst
Teorien utviklet av Volmer forklarer hvordan veksten av en krystall foregår, og fastslår at, rundt den grunnleggende strukturen fra kimdannelsen til det krystallinske stoffet, en slags absorpsjonslag, som fungerer som et grensesnitt, og i tillegg til dette, fremmer det en migrasjon av partikler rundt den, som beveger seg parallelt med overflaten. Resultatet av denne prosessen er definert som en struktur definert i et todimensjonalt plan.
For deres del bestemte Kossel og Straski det mekanisk arbeid er påkrevd for å oppnå fiksering av et ion til overflaten av dette laget, og at det avhenger av dets posisjon.
Utviklingen av en modell som definerer vekst krever prognose for metningssoner der en høyere endringsrate observeres (lokale overmettingssoner). Dette viser at krystallvekst forekommer i lag.
Krystallisering som en separasjonsmekanisme
Siden en krystall er dannet med en homogen substans, har bruken av den som en metode for selektiv separasjon av stoffer spredt seg, blant flere metoder nedenfor, og vil forklare hva de hvis bruk er mer utbredt består av:
- Tilsette et nytt løsemiddel: Hvis vi kjenner til produktene vi håndterer, kan vi bruke denne metoden, som i utgangspunktet består i å tilsette et nytt løsningsmiddel som samhandler med løsningsmidlet der løsemiddelet som vi ønsker å krystallisere er nedsenket. Når det nye løsningsmidlet selektivt begynner å samhandle med sin homolog, faller det oppløste stoffet ut, og initierer krystalliseringsprosessen.
- Kjøling til høye konsentrasjoner av oppløste stoffer: Når vi har en høy-konsentrasjonsløsning, som ble laget ved høye temperaturer, og vi underkaster den en avkjølingsprosess, oppnår vi en tilstand av overmetting, der en større mengde oppløst stoff er oppløst enn løsningsmidlet kan akseptere, i de nye temperaturforhold. Hvis prosessen med å redusere temperaturen skjer på en kontrollert måte, kan vi påvirke størrelsen på krystallet vi skal oppnå.
- Sublimering: Denne teknikken kan bare brukes i krystallinske forbindelser som har høyt damptrykk, på en slik måte at transformasjonene fra en gassfase til en fast ikke krever passering gjennom smeltepunktet.