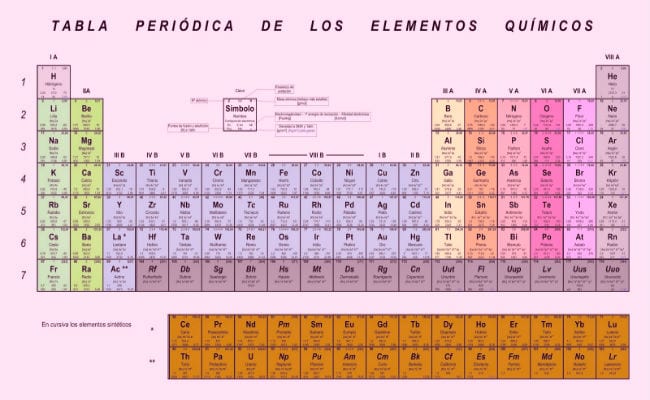
Jedným z veľkých úspechov na vedeckej úrovni bola klasifikácia a organizácia prvkov. Štúdium vlastností hmoty sa datuje do čias alchymistov, vedci v tejto oblasti mali vždy na pamäti dôležitosť vytvorenia klasifikačného systému, ktorý by umožňoval usporiadané spravovanie v tej dobe známych prvkov.
Odtiaľ sa po mnohých pokusoch vyvinula známa tabuľka elektronegativít, známa tiež ako Mendelejevova periodická tabuľka, čo je najefektívnejší systém klasifikácie a organizácie, aký doteraz máme. V ňom sú prvky usporiadané dovnútra funkcie ich elektronegativít, čo je miera schopnosti elektrónov jeho poslednej škrupiny kombinovať sa s inými atómami, ale o tom si ešte povieme.
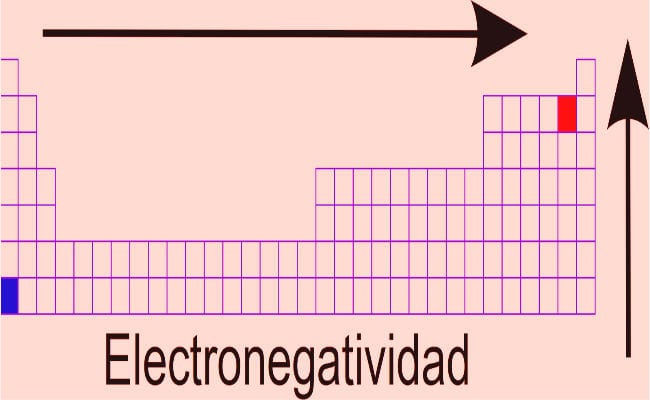
Čo je elektronegativita?
Predtým, ako sa budeme podrobne venovať tejto téme, je dôležité si ujasniť, že všetka hmota sa skladá z atómov, ako ich definoval John Dalton v roku 1803. Atóm je elementárna a nedeliteľná jednotka hmoty, ktorá sa skladá z jadra, okolo ktorého sú elektróny a protóny rotujú na eliptických dráhach a sú to práve elektróny prítomné v poslednej vrstve prvku v jeho stave agregácie. určuje kapacitu každého materiálu za vzniku zlúčenín. To je to, čo definuje elektronegativitu, schopnosť atómu kombinovať sa prostredníctvom väzieb s inými atómami.
Tento proces je definovaný pôsobením dvoch veličín:
- Atómová hmotnosť: Aká je celková hmotnosť protónov a neutrónov v jednom atóme.
- Valenčné elektróny: Negatívne nabité častice nachádzajúce sa v poslednej vrstve atómu, ktoré tvoria množstvo častíc dostupných na uskutočnenie výmeny pri tvorbe zlúčenín.
Vývoj tabuľky elektronegativity
Pri hľadaní adekvátnej klasifikácie prvkov vyvinuli mnohí vedci predstavy o tom, čo by mohlo byť vhodným systémom, prostredníctvom ktorého by bolo možné k prvkom dostať riadnym spôsobom pri zohľadnení ich vlastností. Nasledujúci vedci významne prispeli k vytvoreniu súčasnej tabuľky elektronegativít:
- Antoine Lavoisier: Klasifikácia prvkov týmto vedcom bola vykonaná ľubovoľne bez zohľadnenia akýchkoľvek klasifikačných kritérií, takže jeho klasifikácia nebola veľmi úspešná.
- Johann Doberiner: Tento vedec je známy vývojom triád, ktoré nesú jeho meno. Vypracoval štúdiu, v ktorej zoskupil prvky do skupiny troch, pričom porovnaním zistil, že ich relatívne atómové hmotnosti (ktoré sa stanovujú pomocou hmotnostného spektrometra) a určité hodnoty ich fyzikálnych vlastností navzájom súviseli. Dali sa preto predpovedať pomocou matematických aproximácií. Britský chemik John newlands, pracoval na základe vyvinutom Dobereinerom, a tak sa mu podarilo usporiadať prvky do tabuľky so zoskupeniami prvkov relatívnych atómových hmotností v rastúcej podobe; Týmto zoskupením sa Briti snažili vyvinúť tabuľku, ktorá by obsahovala vzor pravidelných opakovaní fyzikálne vlastnosti prvkov. Pretože takéto opakovania boli zoskupené okolo 8 prvkov, boli označené názvom "Zákon oktáv".
- Lothar Mayer: Je známy rozširovaním vedomostí v oblasti štúdia vzťahu fyzikálnych vlastností a atómových vlastností zložiek. Jeho tvorba bola doplnkom k práci, ktorú produkoval Mendelejev, a bola na ňom nezávislá.
- Dmitrij Mendeleev: Na základe postulátov periodický zákon, tento vedec vyvinul najúspešnejšiu prácu s klasifikáciou prvkov, ktorá je stále v platnosti (s úpravami, do ktorých boli pridané nové objavené prvky. Klasifikoval prvky s prihliadnutím na ich elektronegativitu a mal víziu ponechať skrinky tam, kde žiadny prvok nie je fit, predpokladajúc, že by sa tam zmestil prvok, ktorý ešte nebol objavený. Známe prvky, ktoré unikli parametrom objednávky, boli zaznamenané osobitne, namiesto svojvoľného zahrnutia (chyba, ktorú urobili Lavoisier a Newlands). Pokiaľ ide o elektronegativitu v tabuľke, všeobecné pravidlo je: Elektronegativita je hodnota, ktorá sa zvyšuje, keď sa pohybujeme vpravo od tabuľky, pričom pozorujeme pokles, keď sa pohybujeme doľava. Prvky v hornej časti tabuľky majú vyššie hodnoty elektronegativity.
Váhy elektronegativity
Rozdielne hodnoty elektronegativity určujú typ vytvorenej väzby, preto bola štúdia tohto procesu predmetom záujmu a boli vyvinuté dva postuláty:
Paulingova stupnica: Podľa Paulingových štúdií sa zistilo, že elektronegativita je premenlivá vlastnosť, pretože závisí od oxidačného stavu prvku. Jeho pozorovania mu umožnili určiť, že ak dôjde k odčítaniu alebo rozdielu elektronegativít, mohli by sme predpovedať typ väzby, ktorá by sa vytvorila, pretože vytvoril stupnicu:
- Iónová väzba: Gradient elektronegativity väčší alebo rovný 1.7. Táto väzba sa zvyčajne vyskytuje medzi kovovými a nekovovými prvkami.
- Kovalentná väzba: Keď je rozdiel v rozmedzí 1.7 až 0.4. Je bežné vidieť ich v nekovových zlúčeninách.
- Polárny odkaz: Pre rozdiely rovné alebo menšie ako 0.4.
Mullikenova stupnica: Je založená na elektronickej afinite prvkov, ktorá definuje ich tendenciu získavať negatívny náboj, čo definuje schopnosť prvku prijímať elektróny. Pracuje tiež s iónovými potenciálmi, ktoré následne určujú predispozíciu prvku k prijatiu kladného náboja (kladne nabitými prvkami sú tie, ktoré darujú elektróny zo svojej poslednej škrupiny). Táto stupnica pracuje s priemernými hodnotami.