في الكيمياء ، هناك عناصر لا حصر لها قد تكون مرتبطة ببعضها البعض أو لا. هناك معادن ، لافلزات ، لانثانيدات وأكتينيدات ، معادن انتقالية وأتربة قلوية ؛ وبالطبع لدينا أحد العناصر الكيميائية الذين نوليهم القليل من الاهتمام خلال دروس الكيمياء ، وأقل بكثير عندما يتعلق الأمر بمواصلة حياتنا. أنا أتحدث بالطبع عن الغازات النبيلة.
هذه العناصر ، نظرًا لكونها نادرة جدًا في البيئة ، لا يمكننا تحليلها كثيرًا. هنا سوف نتعرف على تاريخ الغازات النبيلة ، واستخداماتها وخصائصها ، بالإضافة إلى الأشياء الغريبة الأخرى. ابق هنا وتعلم أروع الأشياء عن الغازات النبيلة.
دعنا نتعرف على الغازات
إنها مجموعة من المركبات الكيميائية لها خصائص متشابهة جدًا مع بعضها البعض. على سبيل المثال ، في ظل الظروف العادية ، تكون غازات عديمة اللون والرائحة وأحادية الذرة ولها تفاعل كيميائي منخفض للغاية. تقع هذه في المجموعة رقم 18 من الجدول الدوري ، وتعرف باسم: الهيليوم ، النيون ، الزينون ، الأرجون ، الكريبتون ، المشع: الرادون ، والاصطناعي: Oganeson.
يمكن تفسير خصائصه من خلال النظريات الحديثة الموجودة حول التركيب الذري. تعتبر غلاف إلكترونات التكافؤ الخاصة بهم كاملة ، مما يمنحهم ميلًا محدودًا للمشاركة في التفاعلات الكيميائية ، وهو أحد أسباب سوء فهمهم. في الواقع ، تم تحضير عدد قليل جدًا من مركبات الغازات النبيلة حتى يومنا هذا.
من أين نحصل على الغازات النبيلة؟
نحصل على النيون والأرجون والزينون والكريبتون من الهواء باستخدام طرق التقطير الجزئي والإسالة. يوجد الهيليوم في الغاز الطبيعي ، حيث يجب فصلها بشكل نموذجي. ويتم الحصول على الرادون من خلال التحلل الإشعاعي للمركبات المذابة في الراديوم.
و Oganeson هو عنصر اصطناعي تم إنشاؤه في عام 2002 ، والذي حصل على تسميته IUPAC في عام 2016. وهو معروف بكونه تفاعليًا تمامًا وكذلك غير مستقر ، لذلك لم يتم القيام بالكثير من العمل معه.
كان لهذه الغازات استخدامات مهمة جدًا في مجالات الإضاءة واللحام واستكشاف الفضاء. يستخدم Trimix ، وهو محلول من الهيليوم والأكسجين والنيتروجين ، بحيث لا يعاني الغواصون من التأثير المخدر للنيتروجين في الأعماق. ما هو أكثر من ذلك ، بعد معرفة مخاطر قابلية الهيدروجين للاشتعال ، تم استبدال هذا بالهيليوم في إنشاء المناطيد وبالونات الهواء الساخن.
خصائص هذه الغازات
حصلت الغازات النبيلة على اسمها من الترجمة الألمانية إديلجاس، الاسم الذي استخدمه الكيميائي Hugo Erdman لأول مرة في عام 1898. بهذا الاسم سعى للإشارة إلى معدل التفاعل المنخفض من هذه العناصر. في الواقع ، هذه هي العناصر الأقل تفاعلية المعروفة ، لدرجة أنها تكون خاملة أو غير تفاعلية.
هذا لأن لديهم غلاف تكافؤ كامل يجعلهم يتمتعون بقدرة منخفضة على إطلاق الإلكترونات ويجعل سلوكهم قريبًا من سلوك الغاز المثالي.
بشكل عام ، تشترك الغازات النبيلة في خصائص مختلفة.
- هم عناصر غير معدنية: كونها غازات ، لا تحتوي على أي جسيم معدني في شكلها. في نفس الوقت هم غير قادرين على التفاعل مع المعادن الأخرى.
- هم عديم اللون والرائحة: على الرغم من أنه يمكن إعطاؤها ألوان المصابيح والمصابيح تم إنشاؤها بواسطة هذه الغازات باستخدام الكهرباء ، فهي في الأصل عديمة اللون والرائحة.
- لديهم طبقة تكافؤ كاملة: يحتوي النيون والزينون والأرجون والكريبتون والرادون على ثمانية إلكترونات في غلافهم الأخير. من جانبه ، يحتوي الهليوم على إلكترونين. بهذه الطريقة ، تحتوي الغازات النبيلة على غلاف تكافؤ كامل. لهذا السبب ، في ظل الظروف العادية ، لا تشكل هذه العناصر روابط.
- توجد كغازات أحادية: كما هو مفهوم ، فإن هذه العناصر ، حتى أكبرها ذريًا ، لها ذرة واحدة فقط.
- هم عمليا غير رد الفعل: نظرًا لتكافؤهم الكامل وصعوبة توصيل الإلكترونات ، فإنهم يعتبرون خاملًا عمليًا.
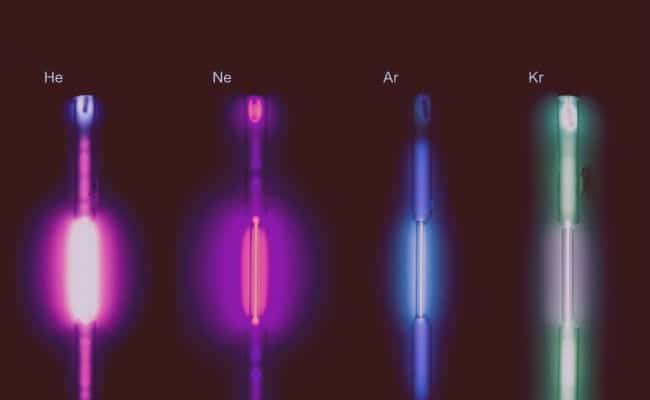
- أنها توصل الكهرباء وتنتج الفلورة: على الرغم من انخفاضها الشديد ، إلا أن هذه الغازات قادرة على توصيل الكهرباء ، وهي بذلك تتوهج بشكل فسفوري.
- لديهم درجة انصهار وغليان منخفضةهذه الغازات النبيلة لها نقاط انصهار وغليان منخفضة للغاية.
- لديهم كهرسلبية منخفضة للغاية: هذه العناصر منخفضة جدا كهرسلبية
- لديهم طاقة تأين عالية: طاقة التأين في الواقع هي الأعلى في دورتك الشهرية.
- فهي ليست قابلة للاشتعال: حتى بسبب كوب الهيدروجين القابل للاشتعال ، تم استبداله بالهيليوم في صناعة المناطيد والبالونات.
كما هو الحال مع التفاعل ، فإن قواها بين الذرية ضعيفة جدًا أيضًا ، وهذا هو سبب انخفاض درجات حرارة انصهارها وغليانها ، وجميعها غازات أحادية الذرة في الظروف العادية ، بما في ذلك الغازات ذات الكتلة الذرية الأعلى.
للهيليوم العديد من الخصائص التي لا يمتلكها أي غاز نبيل آخر أو أي عنصر آخر في الجدول الدوري. له نقطة الانصهار هي الأدنى في جميع العناصر المعروفة ، بالإضافة إلى كونه العنصر الوحيد الذي يمتلك حالة من السيولة الفائقة ؛ حالة تكون فيها المادة في حالة سائلة ، ولكنها يمكن أن تعمل دون فقدان الطاقة الحركية. يحتاج الهيليوم إلى ضغط 25 ميكرون ودرجة حرارة -272 درجة مئوية حتى يتمكن من التصلب.
غلاف التكافؤ الكامل مسؤول أيضًا عن قدرة هذه الغازات على التأين العالية (الأعلى في الجدول الدوري). ولا يمكن تكوين الأيونات بسهولةمما يدل على ثباتها في تكوينها الإلكتروني.
تتناقص طاقة التأين مع تناقص المجموعة ، حيث يزداد نصف القطر الذري وتكون إلكترونات التكافؤ بعيدة عن النواة وبالتالي أقل انجذابًا إليها. هذا يسبب أنه على الرغم من أن فترته هي الأعلى ، إلا أن بعض الغازات النبيلة لها طاقة تأين مماثلة لعناصر أخرى. على سبيل المثال ، طاقة تأين الزينون قابلة للمقارنة مع طاقة التأين للأكسجين.
استخدامات هذه الغازات
من خلال الحصول على نقاط غليان وانصهار منخفضة ، إنها مفيدة بشكل خاص في تصنيع معدات التبريد، ويجعلها مفيدة كمبردات أيضًا.
يستخدم الهيليوم السائل ، الذي يغلي عند 4,2 كلفن (-268,93 درجة مئوية) في تصنيع المغناطيسات فائقة التوصيل ، مثل تلك المستخدمة في التصوير بالرنين المغناطيسي والرنين المغناطيسي النووي.
النيون السائل ، على الرغم من أنه لا يصل إلى درجات الحرارة المنخفضة للهيليوم السائل ، إلا أنه يحتوي على المزيد من التطبيقات في علم التبريد الشديد ، نظرًا لأنه يمتلك القدرة على تبريد 40 مرة أكثر من الهيليوم السائل و 3 مرات أكبر من الهيدروجين السائل.
يستخدم الهيليوم كعنصر من مكونات الغازات القابلة للتنفس ليحل محل النيتروجين ، وذلك بفضله انخفاض الذوبان في السوائلوخاصة في الدهون. يتم امتصاص الغازات في الدم وأنسجة الجسم عند وجود ضغط ، مثل الغوص تحت الماء ، والذي ينتج عنه تأثير مخدر يسمى مرض العمق. نظرًا لانخفاض قابليته للذوبان ، يدخل القليل من الهيليوم إلى أغشية الخلايا ، مما يساعد على الحد من التأثير المخدر.
بسبب قلة احتراقه وخفته ، وبعد كارثة هيندنبورغ عام 1937 ، حل الهيليوم محل الهيدروجين في صناعة الوقود ، على الرغم من فقدان القدرة على الطفو بنسبة 8,6٪.
تستخدم هذه الغازات في الإضاءة بسبب موصليةها. في صناعة المصابيح المتوهجة ، يتم استخدام خليط من الأرجون والنيتروجين لملئها. كريبتون تستخدم في المصابيح عالية الأداءمثل مصابيح الهالوجين ، التي تتميز بدرجة حرارة لون أعلى وفعالية أعلى.
يستخدم Xenon بشكل شائع في مصابيح الزينون الأمامية ، والتي من خلال تحقيق طيف ضوئي مشابه لضوء النهار ، يتم استخدامه في أجهزة عرض الأفلام وكذلك المصابيح الأمامية للسيارة.
في الطب ، يستخدم الهيليوم لتحسين سهولة التنفس لدى مرضى الربو. يمكن استخدام الزينون كمخدر نظرًا لقابليته العالية للذوبان في الدهون ، مما يجعله أكثر فعالية من أكسيد النيتروز المعتاد ، ولأن الجسم يتخلص منه بسهولة ، فإنه يسمح بالشفاء بشكل أسرع.
الحصول على الصور التي تتم عن طريق الرنين المغناطيسي النووي ، لديها زينون جنبا إلى جنب مع الغازات الأخرى. يستخدم الرادون ، وهو شديد النشاط الإشعاعي ومتوفر بكميات ضئيلة فقط ، في العلاج الإشعاعي.
الإنتاج والوفرة
إن وفرة وسهولة الحصول على الغازات النبيلة تتناسب عكسيًا مع عددها الذري. لذلك ، تتناقص وفرة هذه الغازات مع زيادة عددها الذري.
في الكون، الهليوم هو ثاني أسهل عنصر يمكن الحصول عليهبعد الهيدروجين بنسبة كتلة تقارب 24٪. تشكلت معظم كمية الهليوم في الكون عن طريق التخليق النووي البدائي ، لكن كميته تزداد بفضل مشاركة الهيدروجين في التخليق النووي النجمي (وهي عملية تنشأ عن التفاعلات النووية أثناء العملية التطورية للنجوم).
الغازات المتبقية ليست متوفرة أو سهلة الحصول عليها. الرادون ، على سبيل المثال ، يمكن أن يكون شكل في الغلاف الصخري من خلال اضمحلال الراديوم ألفا ؛ وفي الوقت نفسه طور الزينون نظرية تعرف باسم "نظرية الزينون المفقود" بسبب قوتها المنخفضة نسبيًا في الغلاف الجوي.
لنتحدث قليلا عن كل منهما
- شمس بادئة: نظرًا لقلة احتراقها ، ولأنها ثاني أسهل عنصر يمكن الحصول عليه ، فقد تمكنت من استبدال الهيدروجين كعنصر محتمل لملء البالونات والمنطاد ، لأنها لا تنفجر عند ملامستها للنار.
- نيون: يستخدم هذا الغاز ، بسبب تألقه ولونه الأحمر البرتقالي الذي يتم الحصول عليه عند ملامسته للكهرباء ، لأغراض الدعاية والإعلان. من السهل العثور عليها في أضواء النيون. يمكنك أيضًا الحصول على أنابيب ومصابيح نيون بألوان أخرى ، على الرغم من أنها تحتوي بالفعل على غازات أخرى بداخلها.
- أرجون: يستخدم هذا الغاز في المصابيح المتوهجة لأنه لا يتفاعل مع الفتيل تحت ظروف حرارة وضغط عالية. في أنابيب الفلورسنت يولد اللون الأخضر والأزرق. كما أنها تستخدم في المجال الصناعي لتجنب التفاعلات الكيميائية غير المرغوب فيها.
- كريبتون: يستخدم مع الغازات الأخرى في صناعة المصابيح إنارة المطار نتيجة شدة انبعاث الأضواء الحمراء؛ يمكن استخدامه أيضًا في أجهزة عرض السينما. استخدام الكريبتون مفيد أيضًا في جراحة الشبكية بالليزر.
- زينون: الاستخدام الرئيسي لـ Xenon هو تطوير بواعث ضوئية ذات خصائص مبيدة للجراثيم ؛ أنابيب مضيئة ، ومضات تصويرية ، وكذلك في أنابيب الفلورسنت مع القدرة على إثارة ليزر الياقوت.
- غاز الرادون: ينتج هذا الغاز عن التحلل الإشعاعي لليورانيوم إلى الراديو. بسبب هذا ولأنه شديد النشاط الإشعاعي ، فإن له تطبيقات قليلة جدًا في الحياة اليومية.
لتعكس
على الرغم من أنها تتكون إلى حد ما يصعب الحصول عليها في الحالة الطبيعية (باستثناء ، ربما بالنسبة للهيليوم) ، ولأنها تولد أو تسمح ببعض التفاعلات معها ، فإن الغازات النبيلة هي مركبات مهمة يمكننا رؤيتها ، وحتى استخدامها بشكل يومي.
ربما تكون استخداماتهم مقصورة على مجالات محددة ، لكن هذا لا يعني أنها عديمة الفائدة تمامًا. من إضاءة منازلنا بالمصابيح والمصابيح ، إلى حفظ طعامنا عند استخدامه في الثلاجات ، إلى تنقذ الأرواح عند استخدامها في الطبهذه الغازات ، الطبيعية أو الاصطناعية ، لم تظهر بعد كل ما يمكنها أن تفعله لنا. ومن المؤكد أنه مع تقدم البحث ، سيكون استخدامه أكبر بكثير.
ما هي القدرة على التأين؟
وهشاشتها