كان تصنيف العناصر وتنظيمها من الإنجازات العظيمة على المستوى العلمي. تعود دراسة خصائص المادة إلى زمن الخيميائيين ، وكان علماء هذه المنطقة دائمًا يفكرون في أهمية إنشاء نظام تصنيف ، والذي من شأنه أن يسمح بالإدارة المنظمة للعناصر التي كانت معروفة في ذلك الوقت.
من هناك ، وبعد عدة محاولات ، تم تطوير الجدول المعروف للسلبية الكهربية ، والمعروف أيضًا باسم الجدول الدوري لمندليف ، وهو أكثر أنظمة التصنيف والتنظيم كفاءة لدينا حتى الآن. في ذلك يتم ترتيب العناصر في وظيفة كهرسلبيتهموهو مقياس لقدرة إلكترونات غلافه الأخير على الاندماج مع ذرات أخرى ، لكننا سنتحدث عن ذلك.
ما هي الكهربية؟
قبل الخوض في الموضوع بشكل كامل ، من المهم توضيح أن كل المادة تتكون من ذرات ، كما حددها جون دالتون في عام 1803. الذرة هي الوحدة الأولية وغير القابلة للتجزئة للمادة ، والتي تتكون من نواة ، حولها الإلكترونات و تدور البروتونات في مدارات إهليلجية ، والإلكترونات الموجودة في الطبقة الأخيرة من العنصر في حالتها التجميعية هي التي يحدد قدرة كل مادة لتشكيل مركبات. هذا هو ما يحدد الكهربية ، وهي قدرة الذرة على الاندماج من خلال الروابط مع الذرات الأخرى.
يتم تحديد هذه العملية من خلال عمل كميتين:
- الكتلة الذرية: ما هي الكتلة الكلية للبروتونات والنيوترونات في ذرة واحدة؟
- إلكترونات التكافؤ: الجسيمات سالبة الشحنة الموجودة في الطبقة الأخيرة من الذرة ، والتي تشكل كمية الجسيمات المتاحة لإجراء التبادل في تكوين المركبات.
تطوير جدول الكهربية
في بحثهم عن التصنيف المناسب للعناصر ، طور العديد من العلماء أفكارًا حول ما يمكن أن يكون نظامًا مناسبًا ، يمكن من خلاله الوصول إلى العناصر بطريقة منظمة ، مع مراعاة خصائصها. قدم العلماء التالية أسماؤهم مساهمات مهمة ساهمت في تطوير الجدول الحالي للسلطات الإلكترونية:
- أنطوان لافوازييه: تم التصنيف الذي أجراه هذا العالم للعناصر بشكل تعسفي ، دون مراعاة أي معايير تصنيف ، لذلك لم يكن تصنيفه ناجحًا للغاية.
- يوهان دوبرينير: يُعرف هذا العالم بتطوير الثلاثيات التي تحمل اسمه. طور دراسة قام فيها بتجميع العناصر في مجموعة من ثلاثة ، واكتشف عن طريق إجراء مقارنات أن كتلها الذرية النسبية (التي يتم تحديدها باستخدام مطياف الكتلة) ، وقيم معينة من خصائصها الفيزيائية ، كانت مرتبطة ببعضها البعض. لذلك ، يمكن التنبؤ بها عن طريق التقريبات الرياضية. كيميائي بريطاني جون نيولاندز، عملت على الأساس الذي طوره دوبرينير ، وبالتالي تمكنت من ترتيب العناصر في جدول مع مجموعات من العناصر ذات الكتل الذرية النسبية في شكل متزايد ؛ مع هذه المجموعة ، سعى البريطانيون إلى تطوير جدول به نمط من التكرارات الدورية لـ الخصائص الفيزيائية للعناصر. نظرًا لأن هذه التكرارات تم تجميعها حول 8 عناصر ، فقد تم الإشارة إليها باسم "قانون الأوكتاف".
- لوثار ماير: وهو معروف بتوسيع المعرفة في مجال دراسة العلاقة بين الخصائص الفيزيائية والخصائص الذرية للمكونات. كان عمله مكملًا ومستقلًا بدوره عن عمل منديليف.
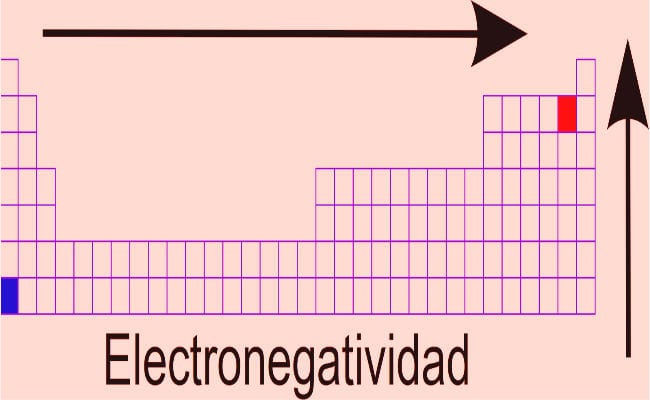
- دميتري مندليف: بناءً على افتراضات قانون دوريطور هذا العالم أنجح أعمال تصنيف العناصر ، والتي لا تزال سارية (مع التعديلات ، حيث تمت إضافة العناصر المكتشفة الجديدة. وصنف العناصر مع مراعاة سلبيتها الكهربية ، وكان لديه رؤية لترك مربعات حيث لا يوجد عنصر مناسب ، مع توقع أن يكون هناك عنصر لم يتم اكتشافه بعد. تمت الإشارة إلى العناصر المعروفة التي تهرب من معلمات الطلب بشكل منفصل ، بدلا من أن يتم تضمينها بشكل تعسفي (خطأ ارتكبه لافوازييه ونيولاندز). فيما يتعلق بالسلبية الكهربية داخل الجدول ، فإن القاعدة العامة هي: الكهربية هي قيمة تزداد كلما انتقلنا إلى يمين الجدول ، مع ملاحظة انخفاض عند الانتقال إلى اليسار. العناصر الموجودة في الجزء العلوي من الجدول لها قيم كهرسلبية أعلى.
مقاييس الكهربية
تحدد القيم المختلفة للسلبية الكهربية نوع الرابطة المتكونة ، وبالتالي ، كانت دراسة هذه العملية هي موضوع الاهتمام ، وتم تطوير افتراضين:
مقياس بولينج: وفقًا لدراسات بولينج ، فقد ثبت أن الكهربية خاصية متغيرة ، لأنها تعتمد على حالة أكسدة العنصر. سمحت له ملاحظاته بتحديد أنه إذا تم إجراء طرح أو اختلاف في الكهرسلبية ، فيمكننا التنبؤ بنوع الرابطة التي سيتم تشكيلها ، منذ أن أنشأ مقياسًا:
- الرابطة الأيونية: التدرج الكهربية أكبر من أو يساوي 1.7. تحدث هذه الرابطة عادة بين العناصر المعدنية وغير المعدنية.
- الرابطة التساهمية: عندما يكون الفرق في النطاق من 1.7 إلى 0.4. من الشائع رؤيتها في المركبات غير المعدنية.
- الرابط القطبي: للاختلافات التي تساوي أو تقل عن 0.4.
مقياس موليكن: يعتمد على التقارب الإلكتروني للعناصر ، والذي يحدد ميلها للحصول على شحنة سالبة ، وهو ما يحدد قدرة العنصر على قبول الإلكترونات. تعمل أيضًا مع الجهود الأيونية ، والتي بدورها تحدد استعداد العنصر لتولي شحنة موجبة (العناصر المشحونة إيجابًا هي تلك التي تتبرع بالإلكترونات من غلافها الأخير) يعمل هذا المقياس مع القيم المتوسطة.