Maadadu waxay ka kooban tahay walxo yaryar oo aan indhaha aadanaha arki karin, kuwaas oo loo yaqaanno atamyo iyo moleculeyaal kuwaas oo ah qaybaha ugu muhiimsan ee waxa aan maanta naqaanno maaddo ahaan.
Qaybaha aan soo sheegnay badanaa waa galaan habka isku xidhka ee loo yaqaan isku xidhka kiimikada, kuwanna waxaa baranaya kimistariga si loo fahmo kumanaanka geeddi-socodka bayoolojiga ah ee maalin walba horteenna ka dhaca laakiin aan si fudud loo dareemi karin. Iyaga ayaga ayaga oo awooday inay fahmaan inta badan dhacdooyinka adduunka ka dhigaya sida ay tahay.
Waa maxay dammaanadaha kiimikada?

Dhammaan waxyaalaha adduunka ka jira oo ay ku jiraan noolaha, oo ay ka mid yihiin aadanaha, waxay ka kooban yihiin midowga atamyo iyo molikuyuullo qaar oo go’aansada inay ku biiraan iyadoo loo marayo geeddi-socod loo yaqaan isku-xirnaanta kiimikada. Waa la ogyahay in noolaha oo dhan iyo xitaa kuwa aan nooleyn (walxaha aan nooleyn) ay ka kooban yihiin maado, tanina waxay kuxirantahay isku xirnaanta kiimikada si ay awood ugu yeeshaan inay is abuuraan.
Waxay kuxirantahay sida atamka iyo molecules ay isuguxiran yihiin, waxaa macquul ah in la go'aamiyo nooca isku xirnaanta kiimikada ee la daaweynayo, oo kuwa ugu caansan waxaa laga heli karaa ionic, covalent iyo metal bonds, in kastoo laba nooc oo bonds ah la helay. bonds aan si fiican loo aqoon marka ay timaado mawduuca, kuwaas oo ah bonds Bridge Bridge iyo Van der Waals.
Bondhiga kiimikada waxaa loogu yeeraa xoogagga sameeya labo ama in ka badan oo atam ah oo isla jooga waqti cayiman, oo u oggolaanaya isu gudbinta elektarooniga dhexdooda.
Geedi socodka soo jiidashada ee ka dhex dhaca labada atam wax yar oo layaableh laakiin in hadii lagu lafoguro fiiro yar si fudud loo fahmi karo. Waxa ugu weyn ee la ogaado waa in nukliyeerka haysta eedeymaha saxda ah ay ka fogaadaan, laakiin isla markaasna ay soo jiidan karaan mahadnaqa elektaroonigga oo leh lacag diidmo ah oo dusha sare saaran, taas oo dhowr jeer ka weynaan karta xoogga ay leedahay waxay keentaa in nukliyeyaashu fogaadaan.
Marka hawsha isku xidhka kiimikada badanaa dhacdo, haddayna ahayn waqtiga oo dhan atamka qaar ayaa lumiya electronka halka kuwa kalena ay guuleysanayaan, laakiin dhamaadka howsha xasillooni koronto ayaa laga dhex arki karaa inta u dhexeysa ficilka oo dhan.
5ta nooc ee isku xidhka kiimikada
Curaarta kiimikada iyo astaamahooda qaarkood hoos ayaa lagu tusi doonaa si loo fahmo sida ay u shaqeeyaan.

Isku xidhka birta
Nooca noocan ah waxaad ku arki kartaa sida daruur loo abuuray oo isku haysa atamka oo dhan, kaas oo ay sameystaan elektaroonigyada dabacsan. Waxaa lagu arki karaa nidaamkan sida atomku u beddelo elektaroonno iyo ion, halkii uu u dhici lahaa sidii caadiga ahayd, isagoo ka tagaya atom ku xiga.
Isku xidhka biraha ayaa badanaa sameeya shabakado loo tixgeliyo crystalline, kuwaas oo leh isuduwid heer sare ah.
Wejiyada shabakadahaas waxaad ku arkeysaa saddex nooc oo kala duwan oo shabakado crystalline ah, kuwaas oo leh dhibco isku-duwanaan kala duwan oo isbeddelaya iyadoo ku xiran hadba meesha ay joogaan, iyagoo gaaraya 12 dhibcood, 8 dhibcood iyo tan ugu dambeysa oo leh 6 dhibcood, iyada oo aan Si kastaba ha ahaatee, waxaa la sheegay in heerka valence of atamka atamka marwalba wuu yaryahay.
Bonds Ionic
Markii aan ka hadlayno curaarta ionic, waxaan rabnaa inaan tixraacno midowga u dhexeeya atamka oo leh tamar yar oo koronto leh iyo kuwa leh tamar isku nooc ah oo ka weyn kuwa hore, kuwaas oo inta badan ah walxo bir ah iyo walxo aan bir ahayn . Si tan ay u dhacdo waa lagama maarmaan in mid ka mid ah atamka uu lumiyo elektaroonig, kan kalena wuxuu u heli karaa si isdaba joog ah. Sidaa darteed, isku-xidhkaani waxaa lagu tilmaami karaa inuu yahay geedi socod ay laba atam ay leeyihiin soo jiidasho korantada, oo midkoodna uu ka qaybqaato soo jiidasho badan kan kalena soo jiidasho yar.
Waxaa la muujiyey in walxaha aan birta ahayn ay ka maqan yihiin elektaroonig wax soo saarkooda si ay awood ugu yeeshaan wareegga oo dhan waana sababtaas tan darteed waxay noqoneysaa mid qaata hawsha, taas oo loo yaqaan anion.
Curiyeyaasha birta waxaa loo yaqaan 'cations' maxaa yeelay waxay leeyihiin lacag qumman oo ka soo horjeedda anions, maaddaama ay leeyihiin elektaroonig ugu dambeeya curintooda, waxay awood u leeyihiin inay ku xirmaan atamka kale, xaaladdan kuwa aan birta ahayn.
Iyadoo lagu hagayo waxa lagu sifeeyey, waxaa laga garan karaa in noocan ah isku xidhka kiimikada atamka uu soo jiito quwadda electrostatic, sidaa darteedna anion-ka uu soo jiito qafiska, halkaasna ay ku taalo markii laga fiirsan karo marka mid ka mid ah atamyada soo baxaan. halka midka kalena uu nuugayo. Marka xaruntani ay ahaato mid adag, waxay sii ahaaneysaa sidii lagu sharraxay oo xasilloon, laakiin daqiiqadda saxda ah waxaa lagu dhejiyaa jawi qoyan ama sida caadiga ah dareeraha qaarkood, way kala bixi doonaan mar labaad, iyagoo ilaalinaya kharashkooda korantada.
Bonds Covalent
Isku xirnaanta wadajirka ah, atomku waxay awood u leeyihiin inay soo jiitaan oo ay wadaagaan elektaroonigga ama ay u nuugaan sida xaaladaha kor ku xusan, waxaana la muujiyey in markay kuwani dhacaan ay ionyaashu aad u deggan yihiin.
In kasta oo la dhihi karo in xiriiriyeyaasha badankood ay leeyihiin awood ay ku dhaqmi karaan koronto, laakiin kiiskan waxaa soo baxday in qeyb weyn aysan aheyn. Dhammaan walxaha dabiiciga ahi waxay ka kooban yihiin isku xirnaan, maxaa yeelay sidaan kor ku soo sheegnay aad bay u deggan tahay.
Boondhigani waxay leeyihiin qayb u gaar ah oo ku kala geddisan hadday isku darsan tahay iyo haddii kaleba, kuwaas oo loo yaqaan 'bond polar bonds' iyo 'nonpolar bonds' oo sharraxaad kooban laga bixin doono xagga hoose.
Xiriirka wadajirka ah ee 'Polar covalent bond'
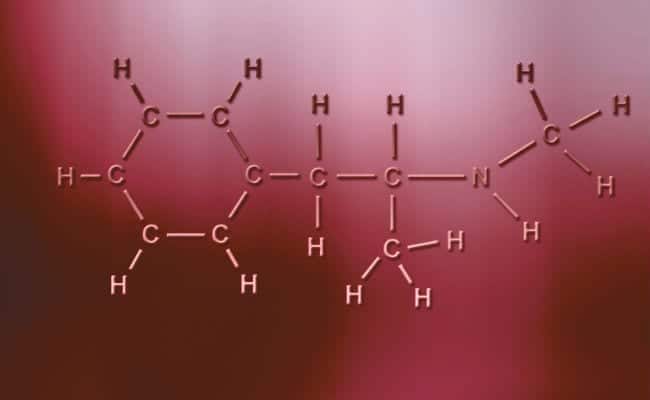
Astaamaha ugu muhiimsan ee isku xidhka wadajirka 'polar covalent bonds' waa inay gabi ahaanba asimmetric yihiin, macnaha atamyada leh qarash togan ama taban waxay yeelan karaan labo elektaroon oo ay wadaagaan ama labo meel oo ay wax kaquuqaan halka midka kale uu leeyahay mid kaliya, kiisaska oo kaladuwan. Kuwani waxay u dhacaan si ficil ahaan la mid ah xirmooyinka ionic laakiin leh farqiga kaliya ee u atomku u midoobayo, isku xirnaansho isku xirnaanta polar ayaa dhacda. Kuwaan si ay u dhacaan waa inay udhaxeeyaan inta udhaxeysa laba shey oo gebi ahaanba ka duwan biraha,
Xiriirka wadajirka ah ee aan caadiga ahayn
Si ka duwan nooca isku xidhka kiimikada ee kor lagu sharaxay, xaaladdan waa inay jirtaa labo ama in ka badan oo atam ah oo aan isku mid ahayn. Tani gebi ahaanba way ka duwan tahay polar-ka dhinac walba, tanna waxaa lagu muujin karaa iyadoo la ogyahay in marka laba atam oo isku cunsur ah ay wadaagaan elektaroonigga maadaama howshu gebi ahaanba is egtahay, waxay ahaanayaan kuwo isku dheelitiran oo labaduba si siman u hela una wada deeqda
Bonds bond bonds
Haydarojiin waxaa lagu gartaa had iyo jeer inay leedahay dano togan, si loo fuliyo dammaanadkan waxaa lagama maarmaan ah inuu ku soo jiito atom at koronto koronto, taas oo mahadsan geeddi-socodkan ay suurtagal tahay in la ilaaliyo sida midowgu u sameysmo inta u dhexeysa laba ka mid ah oo loo qoondeeyay sida buundada hydrogen oo ka timaada halka magaca dammaanaddu ka soo jeedo.
Xiriirinta Van der Waals
Noocyada iskuxiradan, midowga udhaxeeya laba diilimood oo joogto ah ayaa laga heli karaa, iyo sidoo kale inta udhaxeysa laba dileel oo sababa, ama waxaa dhici karta suurtagalnimada in ururada shaqaalaha laga heli doono inta udhaxeysa diifle joogto ah iyo mid sababa. Dariiqa kaliya ee tan ay ku dhici karto waa inta udhaxeysa laba maaddoole oo isu ekaanta, kuwaas oo bilaaba inay ficil sameyaan marka uu jiro soo jiidasho ama naceyb udhaxeeya maaddooyinka ama asal ahaan isdhexgalka u dhexeeya ion iyo molecules.
Waad ku mahadsan tahay daraasadda joogtada ah ee waxay khuseysaa dhammaan noocyada curaarta kiimikada ee jira waa in ay suurtagal noqotay in wax yar laga fahmo sida ay arintu u shaqeyso iyo sida loogu badali karo wax soo saar gebi ahaanba cusub ama ku laaban karto qaabkeedii kadib markii la beddelay ficil isweydaarsiga elektaroniga sida lagu sharaxay inta badan howlahaan.
Aqoontaas oo dhan waxaa lagu gaarey mahadsanida horumarka tikniyoolajiyadda, maadaama markii hore uun la isla dhexmarayey oo ku saabsan jiritaanka atamka iyo tusaalaha tan waa jiritaanka moodellada atomiga ee mufakiriin weyn oo falsafad yaqaan ah, in kasta oo aysan aad uga fogeyn waxa loo yaqaan maanta, maanta waxaa suurtagal noqotay in si fiican loo fahmo hababka.