Једно од великих достигнућа на научном нивоу била је класификација и организација елемената. Проучавање својстава материје датира још из времена алхемичара, научници овог подручја увек су имали на уму важност успостављања система класификације, који би омогућио уредно управљање елементима који су били познати у то време.
Одатле је, после многих покушаја, развијена позната табела електронегативности, позната и као Менделејев периодни систем, што је најефикаснији систем класификације и организације који имамо до сада. У њему су елементи распоређени у функција њихових електронегативности, што је мера способности електрона у последњој љусци да се комбинују са другим атомима, али о томе ћемо разговарати.
Шта је електронегативност?
Пре него што у потпуности пређемо на тему, важно је разјаснити да се сва материја састоји од атома, како је то дефинисао Џон Далтон 1803. Атом је елементарна и недељива јединица материје, која се састоји од језгра, око којег електрони и протони се окрећу у елиптичним орбитама, а то су електрони присутни у последњем слоју елемента у агрегатном стању одређује капацитет сваког материјала да се формирају једињења. То је оно што дефинише електронегативност, способност атома да се комбинује кроз везе са другим атомима.
Овај процес је дефинисан дејством две величине:
- Атомска маса: Колика је укупна маса протона и неутрона у једном атому.
- Валентни електрони: Негативно наелектрисане честице смештене у последњем слоју атома, које чине количину честица доступних за обављање размене у формирању једињења.
Развој табеле електронегативности
У потрази за адекватном класификацијом елемената, многи научници су развили идеје о томе шта би могао бити одговарајући систем, путем којег би се елементима могло уредно приступити, узимајући у обзир њихова својства. Следећи научници дали су важан допринос развоју тренутне табеле електронегативности:
- Антоине Лавоисиер: Класификација елемената коју је извршио овај научник извршена је произвољно, без узимања у обзир било каквих критеријума класификације, тако да његова класификација није била баш успешна.
- Јоханн Добереинер: Овај научник је познат по развоју тријада које носе његово име. Развио је студију у којој је груписао елементе у групу од три, успоређујући да је њихова релативна атомска маса (који се одређују помоћу масеног спектрометра), а одређене вредности њихових физичких својстава биле су међусобно повезане. Стога би се могли предвидети помоћу математичких апроксимација. Британски хемичар Јохн невландс, радио на основи коју је развио Добереинер, и тако успео да нареди елементе у табели са груписањем елемената релативне атомске масе у све већем облику; Овим груписањем, Британци су покушали да развију табелу на којој ће се налазити образац периодичних понављања физичка својства елемената. Пошто су таква понављања била груписана око 8 елемената, означена су именом „Закон октаве“.
- Лотхар Меиер: Познат је по ширењу знања из области проучавања односа физичких својстава и атомских својстава компонената. Његово дело је комплементарно и, заузврат, независно од дела Менделејева.
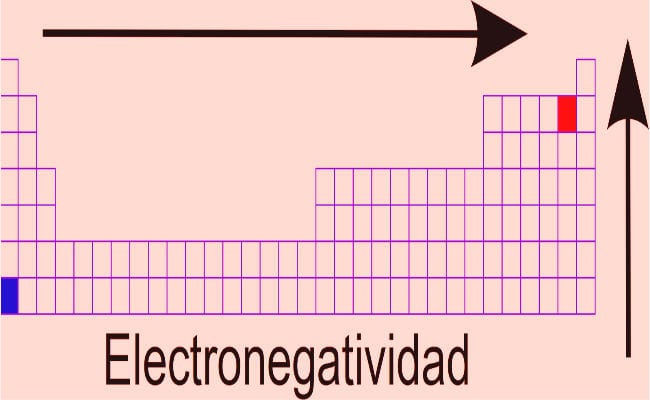
- Дмитри Менделеев: На основу постулата периодични закон, овај научник је развио најуспешније дело класификације елемената, које је и даље на снази (са модификацијама, у које су додани нови откривени елементи. Елементе је класификовао узимајући у обзир њихове електронегативности, и имао је визију остављања кутија тамо где ниједан елемент одговарајући, предвиђајући да ће ту стати елемент који још није откривен. Познати елементи који су избегли параметре реда забележени су одвојено, уместо да буду произвољно укључени (грешку направили Лавоисиер и Невландс). Што се тиче електронегативности у табели, следеће је опште правило: Електронегативност је вредност која се повећава како се померамо десно од стола, примећујући смањење при померању улево. Елементи на врху табеле имају веће вредности електронегативности.
Ваге електронегативности
Различите вредности електронегативности одређују врсту настале везе, па је проучавање овог процеса било предмет интересовања, а развијена су два постулата:
Паулинг скала: Према Паулинговим студијама утврђено је да је електронегативност променљиво својство, јер зависи од оксидационог стања елемента. Његова запажања су му омогућила да утврди да, ако се изврши одузимање или разлика електронегативности, можемо предвидети врсту везе која ће се створити, пошто је успоставио скалу:
- Јонска веза: Градијент електронегативности већи или једнак 1.7. Ова веза се обично јавља између металних и неметалних елемената.
- Ковалентна веза: Када је разлика у распону од 1.7 до 0.4. Уобичајено их је видети у неметалним једињењима.
- Полар линк: За разлике једнаке или мање од 0.4.
Мулликен скала: Заснован је на електронском афинитету елемената, који дефинише њихову тенденцију да стекну негативан набој, што дефинише способност елемента да прихвати електроне. Такође ради са јонским потенцијалима, који заузврат одређују предиспозицију елемента да преузме позитивно наелектрисање (позитивно наелектрисани елементи су они који донирају електроне из своје последње љуске). Ова скала ради са просечним вредностима.