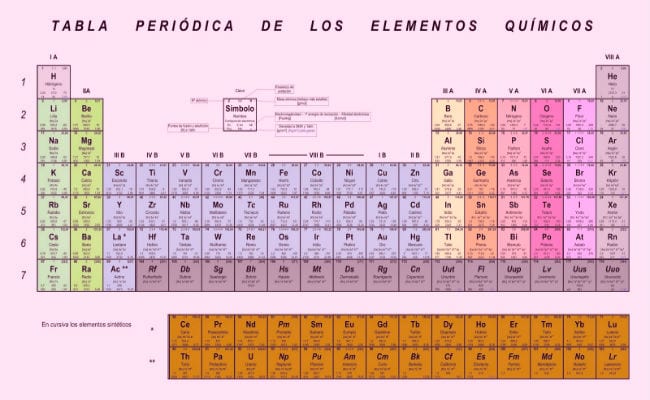
Одним з найбільших досягнень на науковому рівні стала класифікація та організація елементів. Вивчення властивостей речовини бере свій початок з часів алхіміків, вчені цієї області завжди мали на увазі важливість встановлення системи класифікації, яка б дозволяла впорядковане управління елементами, відомими на той час.
Звідти після багатьох спроб була розроблена відома таблиця електронегативів, відома також як періодична система Менделєєва, яка є найефективнішою системою класифікації та організації на сьогоднішній день. У ній елементи розташовані в функція їх електронегативності, що є мірою здатності електронів її останньої оболонки поєднуватися з іншими атомами, але про це ми поговоримо.
Що таке електронегативність?
Перш ніж повністю заглибитися в тему, важливо уточнити, що вся речовина складається з атомів, як це визначив Джон Дальтон в 1803 р. Атом - це елементарна і неподільна одиниця речовини, яка складається з ядра, навколо якого електрони і протони обертаються по еліптичних орбітах, і саме електрони, присутні в останньому шарі елемента в його агрегатному стані, визначає місткість кожного матеріалу утворювати сполуки. Саме це визначає електронегативність, здатність атома поєднуватися через зв’язки з іншими атомами.
Цей процес визначається дією двох величин:
- Атомна маса: Яка загальна маса протонів і нейтронів в одному атомі.
- Валентні електрони: Негативно заряджені частинки, розташовані в останньому шарі атома, становлять кількість частинок, доступних для здійснення обміну при утворенні сполук.
Розробка таблиці електронегативності
У пошуках адекватної класифікації елементів багато вчених розробляли ідеї щодо того, що може бути підходящою системою, за допомогою якої можна отримати доступ до елементів упорядковано з урахуванням їх властивостей. Наступні вчені зробили важливий внесок, який сприяв розробці поточної таблиці електронегативності:
- Антуан Лавуазьє: Класифікація елементів, проведена цим вченим, була проведена довільно, без урахування будь-яких критеріїв класифікації, тому його класифікація не була дуже успішною.
- Йоганн Доберайнер: Цей учений відомий розвитком тріад, які носять його ім’я. Він розробив дослідження, в якому згрупував елементи в групу з трьох, виявивши шляхом порівняння, що їх відносна атомна маса (які визначаються за допомогою мас-спектрометра), а деякі значення їх фізичних властивостей були пов’язані між собою. Тому їх можна було передбачити за допомогою математичних наближень. Британський хімік Джон Ньюлендс, працював на основі, розробленій Доберінером, і таким чином вдалося впорядкувати елементи в таблиці з групуваннями елементів відносної атомної маси у зростаючій формі; За допомогою цього групування британці прагнули розробити таблицю, де б виглядала схема періодичних повторень фізичні властивості елементів. Оскільки такі повтори були згруповані навколо 8 елементів, вони позначалися назвою «Закон октав».
- Лотар Мейєр: Він відомий розширенням знань у галузі вивчення взаємозв'язку фізичних властивостей та атомних властивостей компонентів. Його робота доповнювала і, в свою чергу, не залежала від роботи Менделєєва.
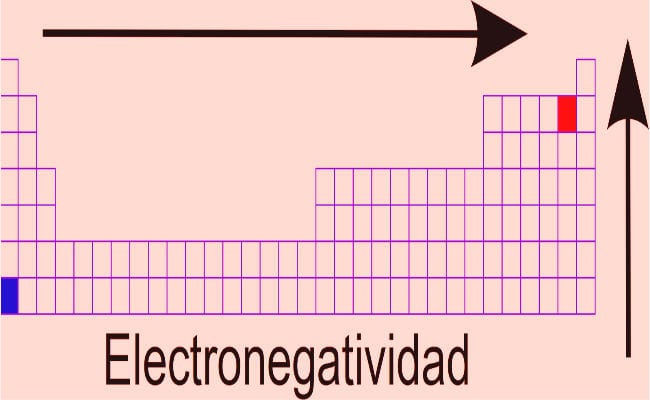
- Дмитро Менделєєв: На основі постулатів періодичний закон, цей вчений розробив найуспішнішу роботу з класифікації елементів, яка діє до цих пір (із модифікаціями, до яких додані нові виявлені елементи. Він класифікував елементи з урахуванням їх електронегативності та мав бачення залишати ящики там, де немає відповідність, передбачаючи, що вміститься елемент, який ще не був виявлений. Відомі елементи, які не відповідали параметрам замовлення, були зазначені окремо, замість довільного включення (помилка, зроблена Лавуазьє та Ньюлендом). Щодо електронегативності в таблиці, загальним правилом є: Електронегативність - це величина, яка збільшується, коли ми рухаємося праворуч від столу, спостерігаючи зменшення при русі ліворуч. Елементи у верхній частині таблиці мають вищі значення електронегативності.
Електронегативні шкали
Різні значення електронегативності визначають тип утвореного зв’язку, отже, вивчення цього процесу було об’єктом інтересу, і було розроблено два постулати:
Шкала Полінга: Згідно з дослідженнями Полінга було встановлено, що електронегативність є змінною властивістю, оскільки вона залежить від ступеня окиснення елемента. Його спостереження дозволили йому визначити, що, якщо буде здійснено віднімання або різницю електронегативності, ми можемо передбачити тип зв'язку, який утвориться, оскільки він встановив шкалу:
- Іонний зв’язок: Градієнт електронегативності більше або дорівнює 1.7. Цей зв’язок зазвичай відбувається між металевими та неметалевими елементами.
- Ковалентний зв’язок: Коли різниця знаходиться в межах від 1.7 до 0.4. Їх часто можна побачити в неметалевих сполуках.
- Полярне посилання: Для різниць, рівних або менше 0.4.
Шкала Муллікена: Він заснований на електронному спорідненості елементів, що визначає їх тенденцію до набуття негативного заряду, що визначає здатність елемента приймати електрони. Він також працює з іонними потенціалами, які, в свою чергу, визначають схильність елемента приймати позитивний заряд (позитивно заряджені елементи - це ті, які віддають електрони з останньої оболонки). Ця шкала працює із середніми значеннями.