Du har helt sikkert nogensinde hørt om krystaller, det er sandsynligt, at dit sind på dette tidspunkt har visualiseret en enorm diamant, en ametyst eller en topas. Og bestemt inkluderer denne gruppe også mange af de kendte "Ædelsten", men en krystal er ikke en betegnelse, der klart omfatter smykkeområdet.
En krystal er slutproduktet af en interessant proces kendt som krystallisation, som er kendetegnet ved at resultere i et homogent fast stof dannet af "ansigter", som er dele placeret i forskellige planer.
Karakteristika for det faste stof fra krystallisation
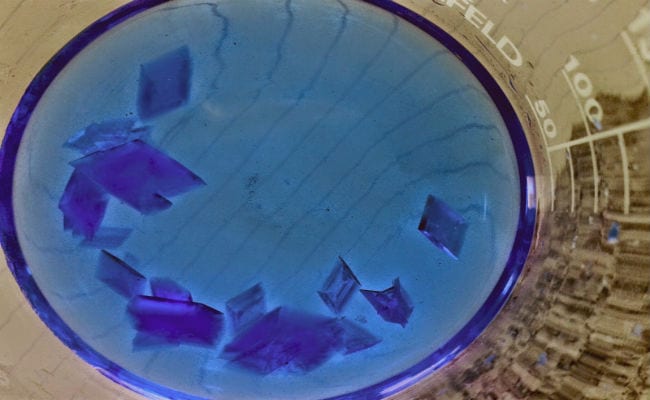
Størrelsen på en krystal er en variabel karakteristik i en lang række dimensioner. "Enorme" krystaller kan findes, som kan måles gennem den lineære enhed "meter", så godt vi kan find krystaller det må være udtrykt som "mikron", da deres lille størrelse gør dem sammenlignelige med mikroorganismer såsom bakterier, som kun kan observeres gennem mikroskopet.
Som nævnt resulterer krystallinske processer i produkter med høj renhed, det er derfor, vi tidligere i definitionen etablerede det krystallerne er homogene: det vil sige, at sammensætningen af produktet forbliver på en konstant værdi på ethvert punkt i det faste stofs volumen, hvilket også indebærer, at de fysiske og kemiske egenskaber forbliver uændrede i hele delen, og i tilfælde af observering af variation på grund af en forstyrrelse, ændringen vil forekomme i hele arten. Denne kvalitet gør krystaller til værdifulde produkter inden for forskellige områder lige fra påskønnelse af materialets kvalitet til anvendelse af krystallisationsprocessen som en teknik til at adskille stoffer.
Krystallinske produkter kan også isoleres på laboratorieniveau gennem kontrollerede reaktioner i samlinger, der efterligner de spontane processer, der forekommer i naturen. En af de største fordele ved krystaller opnået i kontrollerede processer er, at de præsenterer mere regelmæssige former, som perfekt matcher de polygonale figurer med større nøjagtighed.
I en krystal skal vi skelne de ansigter, der er en del af den ægte krystallinske vane (morfologiske egenskaber), og baseret på antallet af dem kan vi overveje de faste grundformer af det faste stof. Normalt i en krystal defineres ved kombinationen af flere grundlæggende formerde vigtigste er følgende:
- Pedion: Glas bestående af et enkelt fladt ansigt uden ækvivalenter.
- Pinacoid: Den består af to ækvivalente ansigter i forhold til en symmetriakse.
- Sphenoid: De to ækvivalente ansigter, der udgør dette solide, ligger omkring en binær akse.
- Prisme: Den består af homologe ansigter, der udgør en zone. At være "et krystalområde" defineret som et sæt ansigter parallelt med den samme retning, svarende til en kant af det samme.
Strukturen af krystaller fra et internt synspunkt kan betragtes som udgjort af et mere eller mindre homogent, periodisk og anisotropisk system af et opløst materiale, der udvikler en struktur på forskellige steder i rummet. Blandt egenskaberne ved krystaller, det faktum, at hvert punkt gentage regelmæssigt i det rum, der er optaget af materialet. I krystallografi kaldes det fænomen, der påvirker denne handling oversættelse.
Krystallisationsproces
For at en krystallisation skal forekomme, skal vi starte med et stof, der kan klassificeres som "Krystallinsk", og dette er defineret, fordi de partikler, der udgør det, uanset om de er af atomær, molekylær eller ionisk natur, har egenskaber af homogenitet, periodicitet og symmetri.
Hele processen aktiveres, når partiklerne på et tidspunkt i det krystallinske stof begynder at omorganisere sig i et stadium kendt som kimdannelse. Hele denne proces involverer, ud over den tydelige variation i rækkefølgen af partiklerne, en proces med ændringer i de termodynamiske forhold, som er orienteret mod kompensationen for de forstyrrelser, der genereres af ændringen i Gibbs fri energi, som er præget af tre begivenheder:
- Ændringen i kemisk energi.
- Oprettelsen af en grænseflade mellem kimdannelseszonen og resten af den homogene fase.
- Variationen i volumen og form, som denne proces involverer, udløser spændinger.
Den næste fase stammer, når kerneafgrænsningsbasestrukturen stabiliseres. Det næste trin er noget logisk og forudsigeligt, når vi først har den grundlæggende struktur, går vi ind i en proces med vækst, hvor en ændring i kernens dimensioner observeres. Lidt efter lidt vil denne stigning resultere i dannelse af ansigter, indtil krystallen får en veldefineret vane.
Mekanisme for krystalvækst
Teorien udviklet af Volmer forklarer, hvordan væksten af en krystal finder sted, idet han fastslår, at omkring den grundlæggende struktur fra kimdannelsen af det krystallinske stof er en slags absorptionslag, som fungerer som en grænseflade, og derudover fremmer den en migration af partikler omkring den, som bevæger sig parallelt med overfladen. Resultatet af denne proces er defineret som en struktur defineret i et todimensionalt plan.
For deres del besluttede Kossel og Straski det der kræves mekanisk arbejde for at opnå fiksering af en ion til overfladen af dette lag, og at det afhænger af dets position.
Udviklingen af en model, der definerer vækst, forudsiger prognosen for mætningszoner, hvor en højere forandringshastighed observeres (lokale zoner med overmætning). Dette viser, at krystalvækst forekommer i lag.
Krystallisering som en separationsmekanisme
Da en krystal er dannet med et homogent stof, har dets anvendelse spredt sig som en metode til selektiv adskillelse af stoffer, blandt flere metoder nedenfor, vil vi forklare, hvad de består, hvis anvendelse er mere udbredt:
- Tilsætning af et nyt opløsningsmiddel: Hvis vi kender arten af de produkter, vi håndterer, kan vi anvende denne metode, som grundlæggende består i at tilføje et nyt opløsningsmiddel, der interagerer med opløsningsmidlet, hvor det opløste stof, som vi vil krystallisere, er nedsænket. Når det nye opløsningsmiddel selektivt begynder at interagere med sin homolog, udfældes det opløste stof og initierer krystallisationsprocessen.
- Køling til høje opløste koncentrationer: Når vi har en opløsning med høj koncentration, der blev fremstillet ved høje temperaturer, og vi udsender den for en afkølingsproces, opnår vi en tilstand af overmætning, hvor en større mængde opløst stof opløses, end opløsningsmidlet kan acceptere, i de nye temperaturforhold. Hvis processen med at reducere temperaturen udføres på en kontrolleret måde, kan vi påvirke størrelsen på krystallen, som vi skal opnå.
- Sublimering: Denne teknik kan kun anvendes i krystallinske forbindelser, der udviser et højt damptryk, på en sådan måde, at transformation fra en gasfase til en fast ikke ikke kræver passage gennem smeltepunktet.