Eine der großen Errungenschaften auf wissenschaftlicher Ebene war die Klassifizierung und Organisation der Elemente. Die Untersuchung der Eigenschaften von Materie geht auf die Zeit der Alchemisten zurück. Die Wissenschaftler dieses Gebiets hatten stets die Bedeutung eines Klassifizierungssystems im Auge, das eine ordnungsgemäße Verwaltung der damals bekannten Elemente ermöglichen würde.
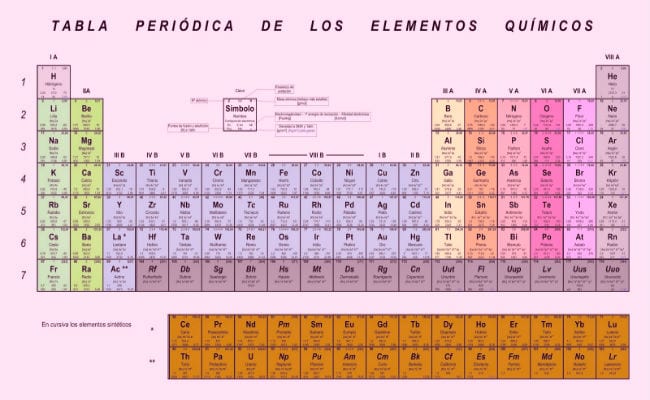
Von dort aus wurde nach vielen Versuchen die bekannte Tabelle der Elektronegativitäten entwickelt, auch bekannt als Mendeleevs Periodensystem, das das effizienteste Klassifizierungs- und Organisationssystem ist, das wir bisher haben. Darin sind die Elemente angeordnet Funktion ihrer ElektronegativitätenDies ist ein Maß für die Fähigkeit der Elektronen in ihrer letzten Schale, sich mit anderen Atomen zu verbinden, aber darüber werden wir sprechen.
Was ist Elektronegativität?
Bevor wir uns vollständig mit dem Thema befassen, ist es wichtig zu klären, dass die gesamte Materie aus Atomen besteht, wie sie 1803 von John Dalton definiert wurde. Das Atom ist die elementare und unteilbare Einheit der Materie, die aus einem Kern besteht, um den sich Elektronen und Elektronen befinden Protonen drehen sich in elliptischen Bahnen, und es sind die Elektronen, die in ihrem Aggregatzustand in der letzten Schicht des Elements vorhanden sind bestimmt die Kapazität jedes Materials Verbindungen zu bilden. Dies ist es, was die Elektronegativität definiert, die Fähigkeit des Atoms, sich durch Bindungen mit anderen Atomen zu verbinden.
Dieser Prozess wird durch die Wirkung von zwei Größen definiert:
- Atommasse: Was ist die Gesamtmasse von Protonen und Neutronen in einem einzelnen Atom?
- Valenzelektronen: Negativ geladene Teilchen in der letzten Schicht des Atoms, die die Menge an Teilchen darstellen, die verfügbar sind, um den Austausch bei der Bildung von Verbindungen durchzuführen.
Entwicklung der Elektronegativitätstabelle
Auf der Suche nach einer angemessenen Klassifizierung der Elemente entwickelten viele Wissenschaftler Ideen für ein geeignetes System, über das unter Berücksichtigung ihrer Eigenschaften auf geordnete Weise auf die Elemente zugegriffen werden kann. Die folgenden Wissenschaftler haben wichtige Beiträge zur Entwicklung der aktuellen Elektronegativitätstabelle geleistet:
- Antoine Lavoisier: Die von diesem Wissenschaftler vorgenommene Klassifizierung der Elemente wurde willkürlich durchgeführt, ohne dass Klassifizierungskriterien berücksichtigt wurden, so dass seine Klassifizierung nicht sehr erfolgreich war.
- Johann Doberiner: Dieser Wissenschaftler ist dafür bekannt, die Triaden zu entwickeln, die seinen Namen tragen. Er entwickelte eine Studie, in der er Elemente in einer Dreiergruppe gruppierte und durch Vergleiche herausfand, dass ihre relativen Atommassen (die mit einem Massenspektrometer bestimmt werden) und bestimmte Werte ihrer physikalischen Eigenschaften wurden miteinander in Beziehung gesetzt. Sie könnten daher mittels mathematischer Näherungen vorhergesagt werden. Britischer Chemiker John Neuland, arbeitete auf der von Dobereiner entwickelten Basis und schaffte es so, die Elemente in einer Tabelle mit Gruppierungen von Elementen relativer Atommassen in zunehmender Form zu ordnen; Mit dieser Gruppierung versuchten die Briten, eine Tabelle zu entwickeln, in der ein Muster von periodischen Wiederholungen der physikalische Eigenschaften der Elemente. Da solche Wiederholungen um 8 Elemente gruppiert waren, wurden sie mit dem Namen bezeichnet "Gesetz der Oktaven".
- Lothar Mayer: Er ist dafür bekannt, sein Wissen auf dem Gebiet der Untersuchung der Beziehung zwischen physikalischen Eigenschaften und atomaren Eigenschaften von Bauteilen zu erweitern. Seine Arbeit war komplementär und unabhängig von der Arbeit von Mendeleev.
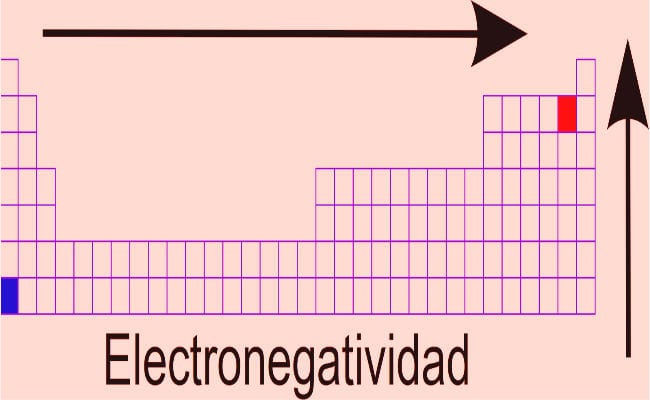
- Dmitri Mendeleev: Basierend auf den Postulaten der periodisches RechtDieser Wissenschaftler entwickelte die erfolgreichste Elementklassifizierungsarbeit, die noch in Kraft ist (mit Modifikationen, bei denen die neu entdeckten Elemente hinzugefügt wurden. Er klassifizierte die Elemente unter Berücksichtigung ihrer Elektronegativitäten und hatte die Vision, Kästchen zu belassen, in denen kein Element vorhanden ist fit, vorausgesetzt, dass ein Element passen würde, das noch nicht entdeckt wurde. Bekannte Elemente, die den Ordnungsparametern entgangen sind, wurden separat notiert. anstatt willkürlich aufgenommen zu werden (Fehler von Lavoisier und Newlands). In Bezug auf die Elektronegativität in der Tabelle lautet die allgemeine Regel: Die Elektronegativität ist ein Wert, der zunimmt, wenn wir uns rechts von der Tabelle bewegen, wobei eine Abnahme beobachtet wird, wenn wir uns nach links bewegen. Die Elemente oben in der Tabelle haben höhere Elektronegativitätswerte.
Elektronegativitätsskalen
Die unterschiedlichen Werte der Elektronegativität bestimmen die Art der gebildeten Bindung. Daher war die Untersuchung dieses Prozesses Gegenstand des Interesses, und es wurden zwei Postulate entwickelt:
Pauling-Skala: Nach Paulings Studien wurde festgestellt, dass die Elektronegativität eine variable Eigenschaft ist, da sie von der Oxidationsstufe des Elements abhängt. Seine Beobachtungen ermöglichten es ihm festzustellen, dass wir, wenn eine Subtraktion oder Differenz der Elektronegativitäten vorgenommen wurde, die Art der Bindung vorhersagen konnten, die sich bilden würde, da er eine Skala festlegte:
- Ionenverbindung: Elektronegativitätsgradient größer oder gleich 1.7. Diese Bindung tritt normalerweise zwischen metallischen und nichtmetallischen Elementen auf.
- Kovalente Bindung: Wenn die Differenz im Bereich von 1.7 bis 0.4 liegt. Es ist üblich, sie in nichtmetallischen Verbindungen zu sehen.
- Polar Link: Für Unterschiede gleich oder kleiner als 0.4.
Mulliken-Skala: Es basiert auf der elektronischen Affinität der Elemente, die ihre Tendenz definiert, eine negative Ladung zu erhalten, was die Fähigkeit eines Elements definiert, Elektronen aufzunehmen. Es funktioniert auch mit Ionenpotentialen, die wiederum die Veranlagung des Elements bestimmen, eine positive Ladung aufzunehmen (positiv geladene Elemente sind solche, die Elektronen aus ihrer letzten Hülle abgeben). Diese Skala arbeitet mit Durchschnittswerten.