Innen kjemi er det utallige elementer som kan eller ikke er relatert til hverandre. Det er metaller, ikke-metaller, lantanider og aktinider, overgangsmetaller og jordalkalier; og selvfølgelig har vi det et av de kjemiske elementene Hvem vi har betalt lite oppmerksomhet i løpet av kjemitimene, og mye mindre når det gjelder å gå videre med livet vårt. Jeg snakker selvfølgelig om edelgasser.
Disse elementene at, da vi er så sjeldne i miljøet, kan vi ikke analysere for mye. Her vil vi lære om edelgassens historie, deres bruk og egenskaper, så vel som andre kuriositeter. Bli her og lær de kuleste tingene om edelgasser.
La oss bli kjent med gassene
De er en gruppe kjemiske forbindelser med veldig like egenskaper til hverandre. For eksempel er de under normale forhold fargeløse, luktfrie, monatomiske gasser og har svært lav kjemisk reaktivitet. Disse er plassert i gruppe 18 i det periodiske systemet, og er kjent som: Helium, neon, Xenon, Argon, Krypton, det radioaktive: Radon, og det syntetiske: Oganeson.
Dens egenskaper kan forklares med eksisterende moderne teorier om atomstruktur. Deres skall av valente elektroner betraktes som komplett, noe som gir dem en begrenset tendens til å delta i kjemiske reaksjoner, og er en av grunnene til at de blir dårlig forstått. Det er faktisk veldig få edelgassforbindelser blitt tilberedt den dag i dag.
Hvor får vi edelgassene?
Vi får neon, argon, xenon og krypton fra luften ved bruk av brøkdestillasjons- og flytende metoder. Helium finnes i naturgass, der den typisk skal skilles. Og radon oppnås ved radioaktivt henfall av forbindelser oppløst i radium.
Og Oganeson er et syntetisk element som ble opprettet i 2002, og som fikk sin IUPAC-nomenklatur i 2016. Det er kjent for å være ganske reaktivt så vel som ustabilt, så det er ikke gjort mye arbeid med det.
Disse gassene har hatt svært viktige bruksområder innen belysning, sveising og romforskning. Trimix, som er en løsning av helium-oksygen-nitrogen, brukes i slik at dykkere ikke lider av den narkotiske effekten av nitrogen i dypet. Hva mer, etter å ha kjent farene for brennbarhet av hydrogen, dette ble erstattet av helium i opprettelsen av luftskip og varmluftsballonger.
Egenskapene til disse gassene
Edelgasser får navnet sitt fra oversettelsen fra tysk edelgas, navnet ble brukt for første gang i 1898 av kjemikeren Hugo Erdman. Med dette navnet søkt å referere til den lave reaktivitetsgraden av disse elementene. Faktisk er dette de minst reaktive elementene som er kjent, så mye at de er praktisk talt inerte eller ikke-reaktive.
Dette er fordi de har et komplett valensskall som etterlater dem med lav kapasitet til å frigjøre elektroner og gjør atferden deres nær den ideelle gassen.
Generelt deler edelgasser forskjellige egenskaper.
- De er ikke-metalliske elementer: Siden den er gass, har den ingen metallpartikler i sin konformasjon. Samtidig er de ikke i stand til å reagere med andre metaller.
- De er fargeløse og luktfrie: selv om de kan gis farger til pærer og lamper opprettet ved hjelp av disse gassene ved bruk av elektrisitet, de er opprinnelig fargeløse og luktfrie.
- De har et fullt valenssjikt: Neon, xenon, argon, krypton og radon har åtte elektroner i sitt siste skall. Helium har på sin side to elektroner. På denne måten har edelgasser et komplett valensskall. Derfor danner disse elementene under normale omstendigheter ikke lenker.
- De eksisterer som monatomiske gasser: Som forstått har disse elementene, selv de største atomene, bare ett atom.
- De er praktisk talt ikke-reaktive: På grunn av deres fulle valens og vanskeligheter med å levere elektroner, blir de ansett som praktisk talt inerte.
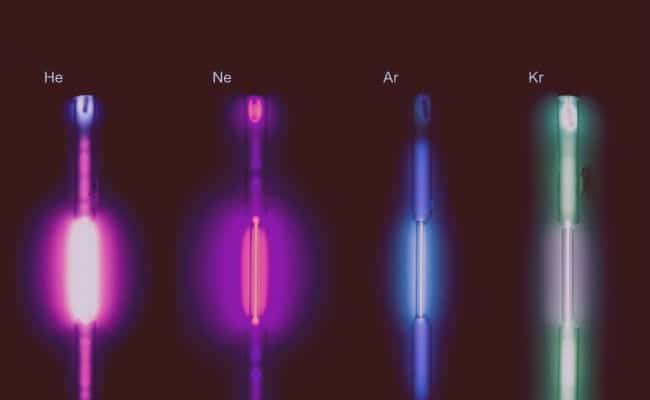
- De leder strøm og produserer fluorescens: Selv om det er veldig lavt, er disse gassene i stand til å lede elektrisitet, og på den måten lyser de fosforesent.
- De har lav smelte- og koketemperaturDisse edelgassene har svært lave smelte- og kokepunkter.
- De har en veldig lav elektronegativitet: disse elementene er veldig lave elektronegative
- De har høy ioniseringsenergi: Din ioniseringsenergi er faktisk den høyeste i din periode.
- De er ikke brannfarlige: Selv på grunn av den brennbare koppen med hydrogen, ble den erstattet av helium ved fremstilling av luftskip og ballonger.
Som med reaktivitet er deres interatomære krefter også veldig svake, og det er derfor de har lave smelte- og koketemperaturer, og de er alle monatomiske gasser under normale forhold, inkludert gasser med høyere atommasse.
Helium har mange egenskaper som ingen annen edelgass eller noe annet element i det periodiske systemet har. Hans smeltepunkt er det laveste i alle de kjente, foruten å være det eneste elementet som eier en tilstand av overflødighet; en tilstand der materie er i flytende tilstand, men kan løpe uten å miste kinetisk energi. Helium trenger et trykk på 25 atm og en temperatur på -272 ºC for å kunne stivne.
Deres fulle valensskall er også ansvarlig for at disse gassene har høy ioniseringskapasitet (den høyeste i det periodiske systemet). og kan ikke danne ioner lett, som viser stabiliteten i den elektroniske konfigurasjonen.
Ioniseringsenergien avtar når gruppen avtar, siden atomradiusen øker og valenselektronene er lenger borte fra kjernen og derfor mindre tiltrukket av den. Dette fører til at selv om perioden er den høyeste, har noen edelgasser det en sammenlignbar ioniseringsenergi til andre elementer. For eksempel er ioniseringsenergien til xenon sammenlignbar med ioniseringsenergien til oksygen.
Bruk av disse gassene
Ved å ha så lave kokepunkter og smeltepunkter, de er spesielt nyttige ved produksjon av kjøleutstyrog gjør dem nyttige som kryogene kjølemidler også.
Flytende helium, som koker ved 4,2 K (-268,93 ºC), brukes til fremstilling av superledende magneter, slik som de som brukes til magnetisk resonansavbildning og kjernemagnetisk resonans.
Flytende neon, selv om det ikke når lave temperaturer av flytende helium, har flere anvendelser innen kryogenikk, siden det har kapasitet til å 40 ganger mer avkjøling enn flytende helium og tre ganger større enn for flytende hydrogen.
Helium brukes som en komponent av pustende gasser for å erstatte nitrogen, takket være dens lav løselighet i væsker, spesielt i lipider. Gasser absorberes i blod og kroppsvev når det er trykk, for eksempel dykking, som gir en bedøvelseseffekt som kalles dybdesyke. På grunn av sin lave løselighet kommer lite helium inn i cellemembranene, noe som bidrar til å dempe den narkotiske effekten.
På grunn av den lave brennbarheten og lettheten, og etter Hindenburg-katastrofen i 1937, erstattet helium hydrogen i produksjonen av drivstoff, til tross for et oppdriftstap på 8,6%
Disse gassene brukes i belysning på grunn av deres ledningsevne. Ved fremstilling av glødepærer brukes en blanding av argon og nitrogen for å fylle dem. Krypton brukes i høyytelsespærerslik som halogenlamper, som har høyere fargetemperatur og høyere effektivitet.
Xenon brukes ofte i xenon-frontlykter, som ved å oppnå et lysspektrum som ligner dagslys brukes i filmprojektorer så vel som billys.
I medisin brukes helium for å forbedre pusteevnen hos astmapasienter. Xenon kan brukes som bedøvelsesmiddel På grunn av den høye løseligheten i lipider, noe som gjør det mer effektivt enn vanlig lystgass, og siden det lett elimineres av kroppen, gir det raskere gjenoppretting.
Fangst av bilder som utføres ved hjelp av kjernemagnetisk resonans, har xenon kombinert med andre gasser. Radon, som er sterkt radioaktivt og bare tilgjengelig i spormengder, brukes i strålebehandling.
Produksjon og overflod
Den overflod og letthet som edelgasser kan oppnås er i omvendt forhold til atomnummeret deres. Derfor reduseres overflod av disse gassene når atomnummeret deres øker.
I universet, er helium det nest enkleste elementet å få, etter hydrogen, med en masseprosent på omtrent 24%. Det meste av heliummengden i universet ble dannet av primær nukleosyntese, men mengden øker takket være deltakelse av hydrogen i stjernenukleosyntese (en prosess som oppstår ved kjernefysiske reaksjoner under stjernens evolusjonære prosess).
Resten av gassene er ikke like store eller enkle å skaffe. Radon, for eksempel, kan være form i litosfæren gjennom alfa forfall av radium; I mellomtiden han xenon har utviklet en teori kjent som "manglende xenon-teori" på grunn av den relativt lave mengden i atmosfæren.
La oss snakke litt om hver
- helium: På grunn av den lave brennbarheten, og fordi det er det nest enkleste elementet å oppnå, har det vært i stand til å erstatte hydrogen som det potensielle elementet for å fylle ballonger og zeppeliner, siden de ikke eksploderer når de kommer i kontakt med ild.
- neon: Denne gassen, på grunn av fluorescens og rød-oransje fargetone som oppnås når den kommer i kontakt med elektrisitet, brukes til reklameformål. Finnes lett i neonlys. Du kan også få neonrør og lamper som har andre farger, selv om de faktisk har andre gasser inni.
- Argon: Denne gassen brukes i glødelamper fordi den ikke reagerer med glødetråden under høye temperatur- og trykkforhold. I lysrør genererer den en grønnblå farge. Det brukes også i industrien for å unngå uønskede kjemiske reaksjoner.
- Krypton: Den brukes sammen med andre gasser i produksjon og produksjon av lamper flybelysning på grunn av intensiteten til de røde lysene som sendes ut; den kan også brukes i kinoprojektorer. Bruk av krypton er også nyttig i retinal laseroperasjon.
- Xenon: den viktigste bruken av Xenon er utarbeidelsen av lysstråler med bakteriedrepende egenskaper; lysrør, fotografiske blink, og også i lysrør med evnen til å opphisse rubinelaseren.
- Radon: Denne gassen genereres ved radioaktivt forfall av uran til radio. På grunn av dette og fordi det er veldig radioaktivt, har det svært få applikasjoner i det daglige.
Å gruble
Selv om de er komponert noe vanskelig å oppnå i naturlig tilstand (bortsett fra, kanskje for helium), og fordi de genererer eller tillater ganske få reaksjoner med dem, er edelgasser viktige forbindelser som vi kan se, og til og med bruke på daglig basis.
Kanskje bruken deres er begrenset til bestemte felt, men det betyr ikke at de er helt ubrukelige. Fra å belyse hjemmene våre i lyspærer og lamper, til å oppbevare maten når den brukes i kjøleskap, til redde liv når det brukes i medisinDisse gassene, naturlige eller syntetiske, har ennå ikke vist alt de kan gjøre for oss. Og det er sikkert at etter hvert som forskningen utvikler seg, vil bruken av den være mye større.
Hva er evnen til ionisering?
og dets skjørhet