En av de store prestasjonene på vitenskapelig nivå var klassifiseringen og organiseringen av elementene. Studien av egenskapene til materie dateres tilbake til alkymistenes tid, forskerne i dette området hadde alltid i tankene viktigheten av å etablere et klassifiseringssystem, som ville tillate ordnet styring av elementene som var kjent på den tiden.
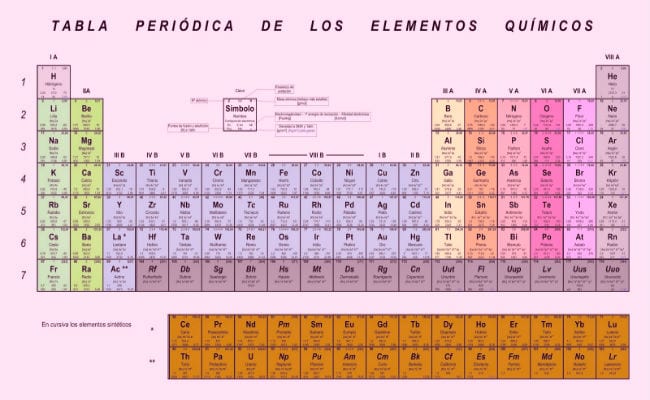
Derfra, etter mange forsøk, ble den velkjente tabellen med elektronegativiteter utviklet, også kjent som Mendeleevs periodiske tabell, som er det mest effektive klassifiserings- og organisasjonssystemet vi har så langt. I den er elementene ordnet i funksjon av deres elektronegativiteter, som er et mål på elektronenes evne til å kombinere med andre atomer, men vi snakker om det.
Hva er elektronegativitet?
Før du går grundig inn i emnet, er det viktig å avklare at all materie består av atomer, som definert av John Dalton i 1803. Atomet er den elementære og udelelige enheten av materie, som består av en kjerne, rundt hvilken elektroner og protoner roterer i elliptiske baner, og det er elektronene som er tilstede i det siste laget av elementet i sin aggregeringstilstand bestemmer kapasiteten til hvert materiale for å danne forbindelser. Dette er det som definerer elektronegativitet, atommets evne til å kombinere gjennom bindinger med andre atomer.
Denne prosessen er definert av handlingen av to størrelser:
- Atommasse: Hva er den totale massen av protoner og nøytroner i et enkelt atom.
- Valenselektroner: Negativt ladede partikler plassert i det siste laget av atomet, som utgjør mengden partikler som er tilgjengelige for å utføre utveksling i dannelsen av forbindelser.
Utvikling av elektronegativitetstabellen
I jakten på en tilstrekkelig klassifisering av elementene utviklet mange forskere ideer rundt hva som kunne være et passende system, der elementene kunne fås tilgang på en ryddig måte, med tanke på egenskapene deres. Følgende forskere ga viktige bidrag som bidro til utviklingen av den nåværende tabellen over elektronegativiteter:
- Antoine Lavoisier: Klassifiseringen laget av denne forskeren av elementene ble utført vilkårlig, uten å ta hensyn til noen klassifiseringskriterier, så klassifiseringen hans var ikke veldig vellykket.
- Johann Doberiner: Denne forskeren er kjent for å utvikle triadene som bærer navnet hans. Han utviklet en studie der han grupperte elementer i en gruppe på tre, og fant ved sammenligning at deres relative atommasser (som bestemmes ved hjelp av et massespektrometer), og visse verdier av deres fysiske egenskaper, var relatert til hverandre. Derfor kunne de forutsies ved hjelp av matematiske tilnærminger. Britisk kjemiker John newlands, arbeidet på basis utviklet av Dobereiner, og klarte dermed å bestille elementene i en tabell med grupperinger av elementer av relative atommasser i økende form; Med denne grupperingen søkte britene å utvikle et bord der et mønster av periodiske repetisjoner av elementers fysiske egenskaper. Siden slike repetisjoner var gruppert rundt 8 elementer, ble de betegnet med navnet "Oktavloven".
- Lothar Mayer: Han er kjent for å utvide kunnskapen innen å studere forholdet mellom fysiske egenskaper og atomare egenskaper til komponenter. Hans arbeid var utfyllende og i sin tur uavhengig av Mendeleevs arbeid.
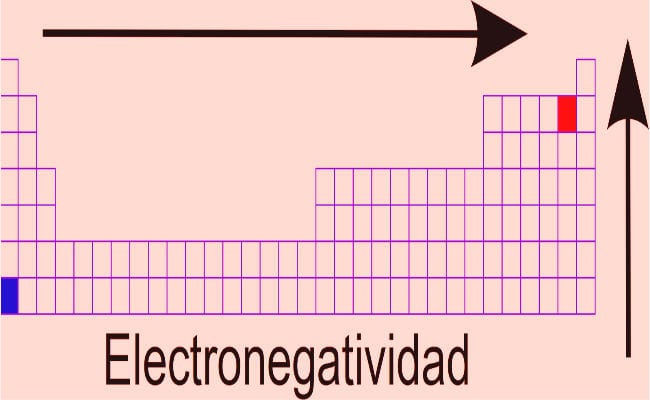
- Dmitri Mendeleev: Basert på postulatene til periodisk lovutviklet denne forskeren det mest vellykkede elementklassifiseringsarbeidet, som fremdeles er i kraft (med modifikasjoner der de nye oppdagede elementene er lagt til. Han klassifiserte elementene under hensyntagen til deres elektronegativiteter, og hadde visjonen om å legge igjen bokser der ingen montert, i påvente av at et element som ennå ikke hadde blitt oppdaget ville passe inn. Kjente elementer som unnslapp ordreparametere ble notert separat, i stedet for å bli inkludert vilkårlig (feil gjort av Lavoisier og Newlands). Når det gjelder elektronegativiteten i tabellen, er den generelle regelen: Elektronegativitet er en verdi som øker når vi beveger oss til høyre for tabellen, og observerer en nedgang når vi beveger oss mot venstre. Elementene øverst på tabellen har høyere elektronegativitetsverdier.
Elektronegativitetsskalaer
De forskjellige verdiene av elektronegativitet bestemmer typen dannet binding, derfor ble studien av denne prosessen gjenstand for interesse, og to postulater ble utviklet:
Pauling skala: I følge Paulings studier ble det slått fast at elektronegativitet er en variabel egenskap, siden den avhenger av oksidasjonstilstanden til elementet. Hans observasjoner tillot ham å fastslå at hvis en subtraksjon eller forskjell mellom elektronegativitetene ble gjort, kunne vi forutsi hvilken type binding som skulle dannes, siden han etablerte en skala:
- Jonisk binding: Elektronegativitetsgradient større enn eller lik 1.7. Denne bindingen forekommer vanligvis mellom metalliske og ikke-metalliske elementer.
- Kovalent binding: Når forskjellen er i området fra 1.7 til 0.4. Det er vanlig å se dem i ikke-metalliske forbindelser.
- Polar lenke: For forskjeller som er lik eller mindre enn 0.4.
Mulliken skala: Det er basert på den elektroniske tilhørigheten til elementene, som definerer deres tendens til å tilegne seg en negativ ladning, som er det som definerer et elementets evne til å akseptere elektroner. Det fungerer også med ioniske potensialer, som igjen bestemmer elementets disposisjon for å ta en positiv ladning (positivt ladede elementer er de som donerer elektroner fra sitt siste skall). Denne skalaen fungerer med gjennomsnittsverdier.