В химии существует бесчисленное множество элементов, которые могут быть связаны друг с другом, а могут и не быть. Есть металлы, неметаллы, лантаноиды и актиниды, переходные металлы и щелочноземельные металлы; и конечно у нас есть один из химических элементов Кому мы уделяли мало внимания на уроках химии, и тем более, когда дело доходит до того, чтобы жить дальше. Я говорю, конечно, о благородных газах.
Эти элементы, которые настолько редки в окружающей среде, что мы не можем слишком много анализировать. Здесь мы узнаем об истории благородных газов, их использовании и свойствах, а также о других диковинках. Останьтесь здесь и узнайте самое интересное о благородных газах.
Давайте познакомимся с газами
Они представляют собой группу химических соединений с очень похожими друг на друга свойствами. Например, при нормальных условиях они бесцветные, одноатомные газы без запаха и имеют очень низкую химическую активность. Они расположены в группе номер 18 периодической таблицы и известны как: Гелий, неон, ксенон, аргон, криптон, радиоактивные вещества: радон и синтетические: оганесон.
Его свойства можно объяснить существующими современными теориями строения атома. Их оболочка из валентных электронов считается законченной, что дает им ограниченную склонность к участию в химических реакциях и является одной из причин, почему они плохо изучены. Фактически, до сих пор было приготовлено очень мало соединений благородных газов.
Где взять благородные газы?
Мы получаем неон, аргон, ксенон и криптон из воздуха методами фракционной перегонки и ожижения. Гелий содержится в природном газе, где его обычно следует разделять. Радон образуется в результате радиоактивного распада растворенных в радии соединений.
Оганесон - это синтетический элемент, созданный в 2002 году и получивший свою номенклатуру IUPAC в 2016 году. Он известен как довольно реактивный, так и нестабильный, поэтому с ним не было проделано много работы.
Эти газы нашли очень важное применение в областях освещения, сварки и исследования космоса. Тримикс, представляющий собой раствор гелий-кислород-азот, используется для того, чтобы дайверы не страдали наркотическим действием азота на глубине. Более того, зная опасность воспламенения водорода, его заменили гелием при создании дирижаблей и воздушных шаров.
Свойства этих газов
Благородные газы получили свое название от перевода с немецкого Эдельгас, имя, впервые использованное в 1898 году химиком Хьюго Эрдманом. С этим именем стремились сослаться на низкую реактивность этих элементов. Фактически, это наименее реактивные из известных элементов, настолько, что они практически инертны или нереактивны.
Это связано с тем, что у них есть полная валентная оболочка, которая не дает им высвобождать электроны и делает их поведение близким к поведению идеального газа.
В целом благородные газы обладают разными свойствами.
- Это неметаллические элементы: Будучи газом, он не содержит металлических частиц. В то же время они не способны вступать в реакцию с другими металлами.
- Они не имеют цвета и запаха: хотя их можно дать цвета к лампочкам и лампам Созданные с помощью этих газов с использованием электричества, они изначально не имеют цвета и запаха.
- У них есть полный валентный слой: Неон, ксенон, аргон, криптон и радон имеют восемь электронов в своей последней оболочке. В свою очередь, гелий имеет два электрона. Таким образом, благородные газы имеют полную валентную оболочку. Вот почему в нормальных условиях эти элементы не образуют ссылок.
- Они существуют как одноатомные газы: Понятно, что эти элементы, даже самые большие в атомном отношении, имеют только один атом.
- Они практически не реагируют: Из-за их полной валентности и сложности доставки электронов они считаются практически инертными.
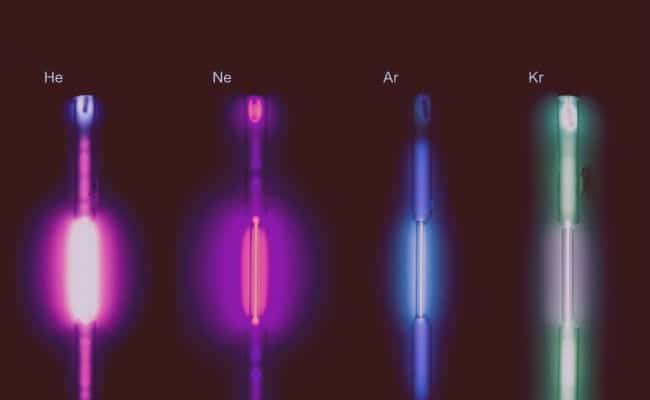
- Они проводят электричество и производят флуоресценцию.: Хотя эти газы очень низкие, они способны проводить электричество и при этом светятся фосфоресцирующим светом.
- У них низкая температура плавления и кипения.Эти благородные газы имеют очень низкие температуры плавления и кипения.
- У них очень низкая электроотрицательность: эти элементы имеют очень низкую электроотрицательность
- Обладают высокой энергией ионизации: Ваша энергия ионизации на самом деле самая высокая за ваш период.
- Они негорючие: Даже из-за легковоспламеняющейся чашки водорода его заменили гелием при производстве дирижаблей и воздушных шаров.
Как и в случае с реакционной способностью, их межатомные силы также очень слабы, поэтому они имеют низкие температуры плавления и кипения, и все они являются одноатомными газами при нормальных условиях, включая газы с более высокой атомной массой.
Гелий обладает многими свойствами, которых нет ни у одного другого благородного газа или любого другого элемента в таблице Менделеева. Его точка плавления самая низкая во всех известных, кроме того, что это единственный элемент, который владеет состоянием сверхтекучести; состояние, в котором вещество находится в жидком состоянии, но может работать без потери кинетической энергии. Гелий должен затвердеть при давлении 25 атм и температуре -272ºC.
Их полная валентная оболочка также отвечает за то, что эти газы обладают высокой ионизационной способностью (самой высокой в периодической таблице). и не может легко образовывать ионы, что свидетельствует о его стабильности в электронной конфигурации.
Энергия ионизации уменьшается по мере уменьшения группы, поскольку атомный радиус увеличивается, а валентные электроны находятся дальше от ядра и, следовательно, менее притягиваются к нему. Это приводит к тому, что, хотя его период самый высокий, некоторые благородные газы имеют сопоставимая энергия ионизации к тому из других элементов. Например, энергия ионизации ксенона сравнима с энергией ионизации кислорода.
Использование этих газов
Имея такие низкие температуры кипения и плавления, они особенно полезны при производстве холодильного оборудования., а также делает их полезными в качестве криогенных хладагентов.
Жидкий гелий, который кипит при 4,2 К (-268,93 ° C), используется в производстве сверхпроводящих магнитов, например магнитов для магнитно-резонансной томографии и ядерного магнитного резонанса.
Жидкий неон, хотя он не достигает низких температур жидкого гелия, имеет больше применений в криогенике, поскольку он обладает способностью В 40 раз больше охлаждения, чем у жидкого гелия и в 3 раза больше, чем у жидкого водорода.
Гелий используется в качестве компонента пригодных для дыхания газов для замены азота благодаря его низкая растворимость в жидкостях, особенно липидов. Газы всасываются в кровь и ткани тела при воздействии давления, например, при подводном плавании с аквалангом, вызывая обезболивающий эффект, называемый глубинной болезнью. Из-за низкой растворимости небольшое количество гелия проникает в клеточные мембраны, что помогает сдерживать наркотический эффект.
Из-за его низкой горючести и легкости, а также после катастрофы в Гинденбурге в 1937 году гелий заменил водород в производстве топлива, даже несмотря на потерю плавучести на 8,6%.
Эти газы используются в освещении из-за их проводимости. При изготовлении ламп накаливания для их заполнения используется смесь аргона и азота. Криптон используется в высокоэффективных лампахтакие как галогенные лампы, которые имеют более высокую цветовую температуру и более высокую эффективность.
Ксенон обычно используется в ксеноновых фарах, которые благодаря световому спектру, близкому к дневному, используются в кинопроекторах, а также в автомобильных фарах.
В медицине гелий используется для облегчения дыхания у больных астмой. Ксенон можно использовать как обезболивающее. Благодаря высокой растворимости в липидах, что делает его более эффективным, чем обычная закись азота, и поскольку он легко выводится из организма, он способствует более быстрому восстановлению.
Захват изображений, который осуществляется с помощью ядерного магнитного резонанса, содержит ксенон в сочетании с другими газами. Радон, который очень радиоактивен и доступен только в следовых количествах, используется в лучевой терапии.
Производство и изобилие
Изобилие и легкость, с которой можно получить благородные газы, обратно пропорциональны их атомному номеру. Следовательно, содержание этих газов уменьшается с увеличением их атомного номера.
Во вселенной, гелий - второй элемент, который легче всего получитьпосле водорода с массовой долей примерно 24%. Большая часть гелия во Вселенной образовалась в результате первичного нуклеосинтеза, но его количество увеличивается благодаря участию водорода в звездном нуклеосинтезе (процесс, который возникает в результате ядерных реакций в процессе эволюции звезд).
Остальных газов не так много и их не так просто получить. Радон, например, может быть форма в литосфере через альфа-распад радия; Между тем он ксенон разработал теорию, известную как «теория пропавшего ксенона». из-за его относительно небольшого количества в атмосфере.
Поговорим немного о каждом
- Гелиограф: Из-за его низкой горючести и поскольку это второй элемент по простоте получения, он смог заменить водород в качестве потенциального элемента для наполнения воздушных шаров и дирижаблей, поскольку они не взрываются при контакте с огнем.
- неон: Этот газ из-за его флуоресценции и красно-оранжевого оттенка, получаемого при контакте с электричеством, используется в рекламных целях. Легко найти в неоновых огнях. Вы также можете приобрести неоновые трубки и лампы других цветов, хотя на самом деле в них есть другие газы.
- Аргон: Этот газ используется в лампах накаливания, поскольку он не вступает в реакцию с нитью накала в условиях высокой температуры и давления. В люминесцентных лампах он имеет зелено-синий цвет. Он также используется в промышленности, чтобы избежать нежелательных химических реакций.
- Криптон: Он используется вместе с другими газами при создании и производстве ламп. освещение аэропорта из-за яркости красных огней; также может использоваться в кинопроекторах. Использование криптона также полезно при лазерной хирургии сетчатки.
- Ксенон: Основное применение ксенона - создание излучателей света с бактерицидными свойствами; люминесцентные лампы, фотографические вспышки, а также люминесцентные лампы с возможностью возбуждения рубинового лазера.
- Радон: Этот газ образуется в результате радиоактивного распада урана. Из-за этого и из-за того, что он очень радиоактивен, он имеет очень мало применений в повседневной жизни.
Отражать
Хотя они несколько составлены трудно получить в естественном состоянии (за исключением, возможно, гелия), и поскольку они генерируют или допускают довольно мало реакций с ними, благородные газы являются важными соединениями, которые мы можем видеть и даже использовать ежедневно.
Возможно, их использование ограничено конкретными полями, но это не значит, что они совершенно бесполезны. От освещения наших домов лампочками и лампами до хранения продуктов в холодильниках и спасать жизни при использовании в медицинеЭти газы, природные или синтетические, еще не показали всего, что они могут для нас сделать. И несомненно, что по мере продвижения исследований его использование будет намного шире.
Какая способность ионизировать?
и его хрупкость