Hmota sa skladá z malých častíc, ktoré sú pre ľudské oko neviditeľné, ktoré sa nazývali atómy a molekuly, ktoré sú hlavnými zložkami toho, čo dnes poznáme ako hmotu.
Vyššie uvedené častice sú zvyčajne vstúpiť do procesu spájania známeho ako chemické spájanie, a tieto študuje chémia, aby pochopili tisíce biologických procesov, ktoré sa vyskytujú každý deň pred nami, ale ktoré nemožno ľahko vnímať. Práve vďaka nim dokázali pochopiť väčšinu udalostí, vďaka ktorým je svet taký, aký je.
Čo sú to chemické väzby?

Všetky existujúce veci na svete vrátane živých bytostí, medzi ktorými sú aj ľudské bytosti, sú tvorené spojením niektorých atómov a molekúl, ktoré sa rozhodnú spojiť prostredníctvom procesu známeho ako chemická väzba. Je dobre známe, že všetky živé organizmy a dokonca aj inertné (neživé objekty) sú tvorené hmotou, čo závisí od toho, či sú chemické väzby schopné samy sa vytvoriť.
Podľa toho, ako sú atómy a molekuly spojené, je možné určiť, aký typ chemickej väzby sa lieči, a medzi najbežnejšie patria iónové, kovalentné a kovové väzby, aj keď sa našli dva typy väzieb. Nové väzby, ktoré nie sú veľmi známe, keď sa hovorí o predmete, čo sú väzby vodíkových mostíkov a Van der Waals.
Chemické väzby sa nazývajú tie sily, vďaka ktorým dva alebo viac atómov zostane určitý čas pohromade a ktoré umožňujú prenos elektrónov medzi nimi.
Proces príťažlivosti, ktorý sa vyskytuje medzi dvoma atómami, sa zmení na niečo trochu zvláštne, ale ak sa analyzuje s malou pozornosťou, dá sa ľahko pochopiť. Hlavná vec, ktorú treba vedieť, je, že jadrá, ktoré majú kladné náboje, sa vzďaľujú, ale zároveň ich môžu priťahovať záporne nabité elektróny, ktoré sa nachádzajú na ich povrchu. Ten môže byť pri niekoľkých príležitostiach väčší ako sila, ktorú spôsobuje. jadrá sa vzďaľovať.
Keď proces chemickej väzby nastane zvyčajne, ak nie vždy niektoré atómy strácajú elektróny zatiaľ čo iní vyhrávajú, ale na konci procesu možno pri všetkých pôsobeniach pozorovať elektrickú stabilitu.
5 druhov chemických väzieb
Chemické väzby a niektoré z ich charakteristík budú uvedené nižšie, aby sme pochopili, ako fungujú.

Kovové odkazy
Na tomto type väzby môžete vidieť, ako sa vytvára oblak, ktorý drží celú skupinu atómov pohromade a ktorú tvoria voľné elektróny. Na tomto procese je možné pozorovať, ako sa atómy transformujú na elektróny a ióny, namiesto toho, aby k nim došlo tak, ako by to bolo za normálnych okolností, a zanechali susedný atóm.
Kovové väzby zvyčajne tvoria siete považované za kryštalické, ktoré majú vysoký index koordinácie.
Na tvárach týchto sietí môžete vidieť tri rôzne typy kryštalických sietí, ktoré majú rôzne koordinačné body, ktoré sa menia podľa toho, kde sa nachádzajú, pričom dosahujú 12, 8 a posledný so 6 bodmi. Hovorí sa však, že valenčná úroveň atómov kovov je vždy malá.
Iónové väzby
Keď hovoríme o iónových väzbách, chceme tým označiť spojenie medzi atómami, ktoré majú malú elektrostatickú energiu, s tými, ktoré majú energiu rovnakého typu väčšiu ako tie prvé, ktoré sú zvyčajne kovovým prvkom a nekovovým prvkom . Aby sa tak stalo, je potrebné, aby jeden z atómov mohol stratiť elektróny a druhý ich mohol postupne získavať. Preto sa dá táto väzba označiť ako proces, pri ktorom majú dva atómy elektrostatickú príťažlivosť, pri ktorej sa jeden zúčastňuje s väčšou príťažlivosťou a druhý s menšou príťažlivosťou.
Ukázalo sa, že nekovové prvky nemajú vo svojom zložení elektrón, aby mohli mať celú svoju obežnú dráhu, a práve z tohto dôvodu sa stávajú prijímačom procesu, ktorý sa nazýva anión.
Kovové prvky sú známe ako katióny, pretože majú kladný náboj, ktorý je opakom aniónov. Pretože majú v poslednom zložení elektrón, majú schopnosť viazať sa na ďalšie atómy, v tomto prípade nekovové.
Na základe toho, čo bolo popísané, sa dá odvodiť, že pri tomto type chemickej väzby sú atómy priťahované elektrostatickou silou, a preto anión priťahuje katión, a práve tam je možné pozorovať, keď sa získa jeden z atómov zatiaľ čo druhá absorbuje. Keď táto zlúčenina zostane pevná, zostane opísaná a stabilná, ale v presnom okamihu je umiestnená vo vlhkom prostredí alebo štandardne v nejakej kvapaline, opäť by sa oddelila a zachovala si elektrický náboj.
Kovalentné väzby
V kovalentných väzbách majú atómy schopnosť priťahovať a zdieľať elektróny alebo ich absorbovať ako v prípadoch uvedených vyššie. Ukázalo sa, že keď k nim dôjde, sú ióny oveľa stabilnejšie.
Aj keď sa dá povedať, že väčšina článkov má kapacitu byť vodičmi elektriny, v tomto prípade sa ukazuje, že veľká časť nie je. Celá organická hmota je tvorená kovalentnými väzbami, pretože ako je uvedené vyššie, je oveľa stabilnejšia.
Tieto väzby majú svoje vlastné rozdelenie, ktoré sa líši podľa toho, či ide o čistú zmes alebo nie, ktoré sa nazývajú polárne väzby a ktorých nepolárne väzby budú uvedené nižšie.
Polárna kovalentná väzba
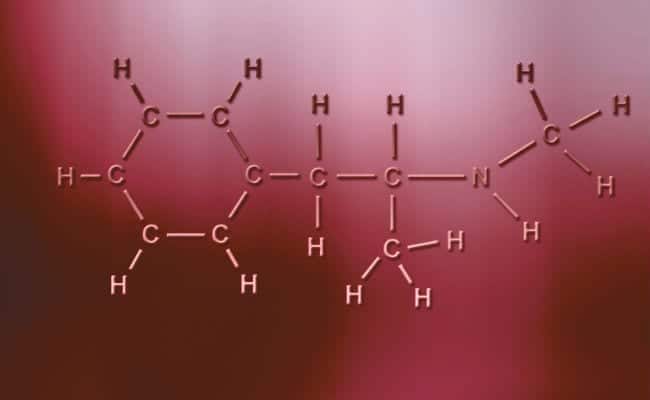
Hlavnou charakteristikou polárnych kovalentných väzieb je to, že sú úplne asymetrické, v tom zmysle, že atómy s kladným alebo záporným nábojom môžu mať spoločné dva elektróny alebo dva priestory, ktoré absorbujú, zatiaľ čo druhý má iba jeden, pričom sa líšia prípady. Dejú sa prakticky rovnako ako iónové väzby, ale s jediným rozdielom, že pri spájaní atómov dochádza k polárnej kovalentnej väzbe. Aby k nim mohlo dôjsť, musí k nim dôjsť medzi dvoma úplne odlišnými nekovovými prvkami,
Nepolárna kovalentná väzba
Na rozdiel od vyššie opísaného typu chemickej väzby musia v tomto prípade existovať dva alebo viac atómov nekovu rovnakého typu. Toto sa vo všetkých ohľadoch úplne líši od polárnych a dá sa to preukázať vedomím, že keď dva atómy toho istého prvku zdieľajú elektróny, pretože proces je úplne symetrický, zostávajú vyvážené a elektróny prijímajú aj darujú rovnako.
Vodíkové väzby
Vodík sa vyznačuje tým, že má vždy kladný náboj a na uskutočnenie tejto väzby je potrebné, aby bol priťahovaný atómom s elektronegatívnym nábojom, ktorý vďaka tomuto procesu umožňuje pozorovať, ako sa vytvára únia medzi dva v jednom, ktorý bol denominovaný ako vodíkový mostík, odkiaľ je odvodený aj názov väzby.
Odkazy na Van der Waals
V tomto type väzieb možno nájsť spojenie medzi dvoma permanentnými dipólmi, ako aj medzi dvoma indukovanými dipólmi, alebo môže existovať možnosť, že sa nájdu spojenia medzi permanentným a indukovaným dipólom. Jediným spôsobom, ako sa to môže stať, je medzi dvoma symetrickými molekulami, ktoré začnú pôsobiť, keď medzi molekulami dôjde k príťažlivosti alebo odpudeniu alebo predvolene dôjde k interakcii medzi iónmi a molekulami.
Vďaka neustálemu štúdiu, že sa vzťahuje na všetky typy existujúcich chemických väzieb spočíva v tom, že bolo možné trochu viac pochopiť, ako hmota funguje a ako sa dá zmeniť na úplne nový produkt alebo sa vrátiť do svojej podoby po zmene akcie výmeny elektrónov, ako je to opísané vo väčšine týchto procesov.
Všetky tieto znalosti boli dosiahnuté vďaka pokroku v technológii, pretože predtým sa iba špekulovalo o existencii atómov a príkladom toho je existencia atómových modelov veľkých filozofických mysliteľov, hoci neboli tak ďaleko od toho, čo je dnes známe, dnes bolo možné procesom lepšie porozumieť.