ภายในเคมี มีองค์ประกอบมากมายที่อาจเกี่ยวข้องหรือไม่เกี่ยวข้องกัน มีโลหะ อโลหะ แลนทาไนด์และแอคติไนด์ โลหะทรานซิชัน และอัลคาไลน์เอิร์ธ และแน่นอนเรามี หนึ่งในองค์ประกอบทางเคมี ผู้ที่เราได้ให้ความสนใจเพียงเล็กน้อยระหว่างชั้นเรียนเคมี และน้อยลงมากเมื่อต้องดำเนินชีวิตต่อไป ฉันกำลังพูดถึงก๊าซมีตระกูล
องค์ประกอบเหล่านี้ซึ่งหายากมากในสิ่งแวดล้อม เราไม่สามารถวิเคราะห์ได้มากนัก ที่นี่เราจะเรียนรู้เกี่ยวกับประวัติของก๊าซมีตระกูล การใช้ประโยชน์และคุณสมบัติของก๊าซ รวมทั้งความอยากรู้อื่นๆ อยู่ที่นี่และเรียนรู้สิ่งที่ยอดเยี่ยมที่สุดเกี่ยวกับก๊าซมีตระกูล
มารู้จักแก๊สกันเถอะ
เป็นกลุ่มของสารเคมีที่มีคุณสมบัติใกล้เคียงกันมาก ตัวอย่างเช่น ภายใต้สภาวะปกติ ก๊าซเหล่านี้ไม่มีสี ไม่มีกลิ่น มีโมเลกุลเดี่ยว และมีปฏิกิริยาเคมีต่ำมาก เหล่านี้อยู่ในกลุ่มที่ 18 ของตารางธาตุและเรียกว่า: ฮีเลียม นีออน ซีนอน อาร์กอน คริปทอน กัมมันตภาพรังสี: เรดอน และสารสังเคราะห์: โอกาเนสัน
คุณสมบัติของมันสามารถอธิบายได้ด้วยทฤษฎีสมัยใหม่ที่มีอยู่เกี่ยวกับโครงสร้างอะตอม เปลือกวาเลนต์อิเล็กตรอนของพวกมันถือว่าสมบูรณ์ ซึ่งทำให้มีแนวโน้มที่จะมีส่วนร่วมในปฏิกิริยาเคมีจำกัด และเป็นหนึ่งในสาเหตุที่ทำให้ไม่เข้าใจพวกมัน อันที่จริงมีการเตรียมสารประกอบก๊าซมีตระกูลน้อยมากจนถึงทุกวันนี้
เราจะหาก๊าซมีตระกูลได้จากที่ไหน?
เราได้รับนีออน อาร์กอน ซีนอน และคริปทอนจากอากาศโดยใช้วิธีการกลั่นแบบเศษส่วนและการทำให้เป็นของเหลว ฮีเลียมมีอยู่ในก๊าซธรรมชาติจาก ที่ควรแยกออกมาต่างหาก. และเรดอนได้มาจากการสลายตัวของสารกัมมันตรังสีของสารประกอบที่ละลายในเรเดียม
และ Oganeson เป็นองค์ประกอบสังเคราะห์ที่สร้างขึ้นในปี 2002 และได้รับระบบการตั้งชื่อ IUPAC ในปี 2016 เป็นที่ทราบกันดีว่ามีปฏิกิริยาตอบสนองและไม่เสถียรดังนั้นจึงไม่มีงานทำมากนัก
ก๊าซเหล่านี้มีประโยชน์อย่างมากในด้านการให้แสงสว่าง การเชื่อม และการสำรวจอวกาศ Trimix ซึ่งเป็นสารละลายของฮีเลียม - ออกซิเจน - ไนโตรเจนถูกนำมาใช้เพื่อให้นักดำน้ำไม่ได้รับผลกระทบจากยาเสพติดของไนโตรเจนในระดับความลึก มีอะไรอีก, หลังจากที่ทราบถึงอันตรายจากการติดไฟของไฮโดรเจนแล้ว นี้ถูกแทนที่ด้วยฮีเลียมในการสร้างเรือบินและบอลลูนอากาศร้อน
คุณสมบัติของก๊าซเหล่านี้
ก๊าซมีตระกูลได้ชื่อมาจากการแปลจากภาษาเยอรมัน เอเดลกัสชื่อที่ใช้เป็นครั้งแรกในปี พ.ศ. 1898 โดยนักเคมี Hugo Erdman ด้วยชื่อนี้ พยายามที่จะอ้างถึงอัตราการเกิดปฏิกิริยาต่ำ ของธาตุเหล่านี้ อันที่จริงองค์ประกอบเหล่านี้เป็นองค์ประกอบที่มีปฏิกิริยาน้อยที่สุดที่รู้จักมากจนแทบไม่มีปฏิกิริยาเลย
เนื่องจากพวกมันมีเปลือกความจุที่สมบูรณ์ซึ่งทำให้พวกมันมีความจุต่ำในการปล่อยอิเล็กตรอนและทำให้พฤติกรรมของพวกมันใกล้เคียงกับก๊าซในอุดมคติ
โดยทั่วไป ก๊าซมีตระกูลมีคุณสมบัติต่างกัน
- เป็นองค์ประกอบที่ไม่ใช่โลหะ: เนื่องจากเป็นแก๊สจึงไม่มีอนุภาคโลหะอยู่ภายในโครงสร้าง ในขณะเดียวกันก็ไม่สามารถทำปฏิกิริยากับโลหะอื่นได้
- ไม่มีสีและไม่มีกลิ่น: แม้จะให้ก็ได้ สีสำหรับหลอดไฟและโคมไฟ เกิดจากก๊าซเหล่านี้โดยใช้ไฟฟ้า แต่เดิมไม่มีสีและไม่มีกลิ่น
- พวกเขามีชั้นความจุเต็ม: นีออน ซีนอน อาร์กอน คริปทอน และเรดอนมีอิเล็กตรอนแปดตัวในเปลือกสุดท้าย ฮีเลียมมีอิเล็กตรอนสองตัว ด้วยวิธีนี้ ก๊าซมีตระกูลจะมีเปลือกความจุที่สมบูรณ์ นั่นคือเหตุผลที่ ภายใต้สถานการณ์ปกติ องค์ประกอบเหล่านี้ไม่สร้างการเชื่อมโยง
- พวกมันมีอยู่ในรูปของก๊าซโมโนโทมิก: ตามที่เข้าใจ องค์ประกอบเหล่านี้ แม้แต่อะตอมที่ใหญ่ที่สุด ก็มีอะตอมเดียวเท่านั้น
- พวกมันแทบไม่มีปฏิกิริยา: เนื่องจากความจุเต็มที่และความยากลำบากในการส่งอิเล็กตรอน พวกมันจึงถือว่าเฉื่อยในทางปฏิบัติ
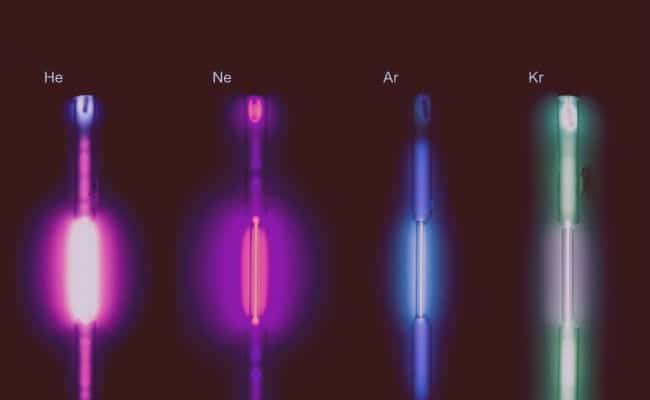
- พวกเขานำไฟฟ้าและผลิตเรืองแสง flu: แม้ว่าจะต่ำมาก แต่ก๊าซเหล่านี้สามารถนำไฟฟ้าได้ และในการทำเช่นนั้น พวกมันจะเรืองแสงเป็นฟอสฟอเรสเซนต์
- มีจุดหลอมเหลวและจุดเดือดต่ำก๊าซมีตระกูลเหล่านี้มีจุดหลอมเหลวและจุดเดือดต่ำมาก
- พวกมันมีอิเล็กโตรเนกาติวีตี้ต่ำมาก: ธาตุเหล่านี้มีค่าอิเล็กโตรเนกาติตีต่ำมาก
- มีพลังงานไอออไนซ์สูง: พลังงานไอออไนเซชันของคุณสูงที่สุดในช่วงเวลาของคุณ
- ไม่ติดไฟ: แม้เนื่องจากถ้วยไฮโดรเจนที่ติดไฟได้ มันถูกแทนที่ด้วยฮีเลียมในการผลิตเรือบินและลูกโป่ง
เช่นเดียวกับการเกิดปฏิกิริยา แรงระหว่างอะตอมของพวกมันก็อ่อนมากเช่นกัน ซึ่งเป็นสาเหตุที่ว่าทำไมพวกมันจึงมีอุณหภูมิหลอมเหลวและจุดเดือดต่ำ และพวกมันเป็นก๊าซโมโนมิกทั้งหมดภายใต้สภาวะปกติ รวมถึงก๊าซที่มีมวลอะตอมสูงกว่า
ฮีเลียมมีคุณสมบัติหลายอย่างที่ไม่มีก๊าซมีตระกูลอื่นหรือองค์ประกอบอื่นใดในตารางธาตุไม่มี ของเขา จุดหลอมเหลวต่ำสุด ในสิ่งที่รู้จักทั้งหมด นอกจากจะเป็นเพียงองค์ประกอบเดียวที่เป็นเจ้าของสถานะของ superfluidity; สถานะที่สสารอยู่ในสถานะของเหลว แต่สามารถทำงานได้โดยไม่สูญเสียพลังงานจลน์ ฮีเลียมต้องการแรงดัน 25atm และอุณหภูมิ -272ºC เพื่อให้สามารถแข็งตัวได้
เปลือกความจุเต็มของพวกมันยังรับผิดชอบต่อก๊าซเหล่านี้ที่มีความจุไอออไนเซชันสูง (สูงสุดในตารางธาตุ) และไม่สามารถก่อตัวเป็นไอออนได้ง่ายซึ่งแสดงความเสถียรในรูปแบบอิเล็กทรอนิกส์
พลังงานไอออไนเซชันจะลดลงเมื่อกลุ่มลดลง เนื่องจากรัศมีอะตอมเพิ่มขึ้นและวาเลนซ์อิเล็กตรอนอยู่ห่างจากนิวเคลียสและดึงดูดน้อยลง ซึ่งทำให้ถึงแม้ช่วงเวลาจะสูงสุด แต่ก็มีก๊าซมีตระกูลอยู่บ้าง พลังงานไอออไนซ์ที่เทียบเคียงได้ กับองค์ประกอบอื่นๆ ตัวอย่างเช่น พลังงานไอออไนเซชันของซีนอนเปรียบได้กับพลังงานไอออไนเซชันของออกซิเจน
การใช้ก๊าซเหล่านี้
โดยมีจุดเดือดและจุดหลอมเหลวต่ำเช่นนี้ มีประโยชน์อย่างยิ่งในการผลิตอุปกรณ์ทำความเย็นและทำให้มีประโยชน์ในฐานะสารทำความเย็นแบบแช่เยือกแข็งเช่นกัน
ฮีเลียมเหลวซึ่งเดือดที่ 4,2K (-268,93ºC) ใช้ในการผลิตแม่เหล็กที่มีตัวนำยิ่งยวด เช่น แม่เหล็กที่ใช้สำหรับการถ่ายภาพด้วยคลื่นสนามแม่เหล็กและคลื่นแม่เหล็กไฟฟ้านิวเคลียร์
นีออนเหลวแม้ว่าจะไม่ถึงอุณหภูมิต่ำของฮีเลียมเหลว แต่ก็มีการใช้งานมากขึ้นในไครโอเจนิกส์เนื่องจากมีความสามารถในการ ระบายความร้อนมากกว่าฮีเลียมเหลวถึง 40 เท่า และไฮโดรเจนเหลว 3 เท่า
ฮีเลียมถูกใช้เป็นส่วนประกอบของก๊าซที่ระบายอากาศได้เพื่อทดแทนไนโตรเจน เนื่องจาก thanks ความสามารถในการละลายต่ำในของเหลวโดยเฉพาะในไขมัน ก๊าซจะถูกดูดซึมเข้าสู่กระแสเลือดและเนื้อเยื่อของร่างกายเมื่อมีแรงกดดัน เช่น การดำน้ำลึก ซึ่งทำให้เกิดอาการชาที่เรียกว่าอาการเจ็บลึก เนื่องจากความสามารถในการละลายต่ำ ฮีเลียมเพียงเล็กน้อยจะเข้าสู่เยื่อหุ้มเซลล์ ซึ่งช่วยลดผลกระทบของยาเสพติด
เนื่องจากความสามารถในการติดไฟและความสว่างต่ำ และหลังจากภัยพิบัติ Hindenburg ในปี 1937 ฮีเลียมแทนที่ไฮโดรเจนในการผลิตเชื้อเพลิง แม้ว่าจะสูญเสียการลอยตัว 8,6%
ก๊าซเหล่านี้ใช้ในการให้แสงสว่างเนื่องจากการนำไฟฟ้า ในการผลิตหลอดไส้จะเติมส่วนผสมของอาร์กอนและไนโตรเจน คริปทอน ใช้ในหลอดไฟประสิทธิภาพสูงเช่นหลอดฮาโลเจนซึ่งมีอุณหภูมิสีสูงกว่าและให้ประสิทธิภาพสูงกว่า
โดยทั่วไปจะใช้ซีนอนในไฟหน้าซีนอน ซึ่งโดยการใช้คลื่นความถี่แสงที่คล้ายกับแสงในเวลากลางวัน จะถูกนำมาใช้ในเครื่องฉายภาพยนตร์และไฟหน้ารถยนต์
ในทางการแพทย์ ฮีเลียมใช้เพื่อทำให้หายใจสะดวกขึ้นในผู้ป่วยโรคหอบหืด ซีนอนสามารถใช้เป็นยาชาได้ เนื่องจากมีความสามารถในการละลายในไขมันสูง ซึ่งทำให้มีประสิทธิภาพมากกว่าไนตรัสออกไซด์ทั่วไป และเนื่องจากร่างกายกำจัดได้ง่ายจึงช่วยให้ฟื้นตัวเร็วขึ้น
การได้มาซึ่งภาพที่ดำเนินการโดยเรโซแนนซ์แม่เหล็กนิวเคลียร์ ได้รวมซีนอนกับก๊าซอื่นๆ เรดอนซึ่งมีกัมมันตภาพรังสีสูงและมีอยู่ในปริมาณน้อยเท่านั้น ถูกนำมาใช้ในการฉายรังสีบำบัด
การผลิตและความอุดมสมบูรณ์
ความอุดมสมบูรณ์และความสะดวกที่จะได้รับก๊าซมีตระกูลอยู่ในสัดส่วนผกผันกับเลขอะตอมของพวกมัน ดังนั้นปริมาณของก๊าซเหล่านี้จึงลดลงเมื่อเลขอะตอมเพิ่มขึ้น
ในจักรวาลฮีเลียมเป็นองค์ประกอบที่ง่ายที่สุดอันดับสองที่จะได้รับหลังไฮโดรเจน โดยมีเปอร์เซ็นต์มวลประมาณ 24% ปริมาณฮีเลียมส่วนใหญ่ในจักรวาลเกิดจากการสังเคราะห์นิวเคลียสในขั้นต้น แต่ปริมาณของฮีเลียมเพิ่มขึ้นเนื่องจากการมีส่วนร่วมของไฮโดรเจนในการสังเคราะห์นิวเคลียสของดาว (กระบวนการที่เกิดขึ้นจากปฏิกิริยานิวเคลียร์ระหว่างกระบวนการวิวัฒนาการของดาว)
ก๊าซที่เหลือมีปริมาณไม่มากหรือหาได้ง่ายนัก เรดอน เช่น สามารถเป็น ก่อตัวในเปลือกโลก ผ่านการสลายตัวของอัลฟาของเรเดียม ในขณะเดียวกันเขา ซีนอนได้พัฒนาทฤษฎีที่เรียกว่า "ทฤษฎีซีนอนที่หายไป" เนื่องจากมีปริมาณค่อนข้างต่ำในบรรยากาศ
มาว่ากันคนละเรื่อง
- ฮีเลียม: เนื่องจากติดไฟได้ต่ำ และเป็นองค์ประกอบที่ง่ายที่สุดอันดับสองที่จะได้รับ จึงสามารถแทนที่ไฮโดรเจนเป็นองค์ประกอบที่มีศักยภาพในการเติมบอลลูนและเรือเหาะ เนื่องจากพวกมันจะไม่ระเบิดเมื่อสัมผัสกับไฟ
- ธาตุนีอ็อน: ก๊าซนี้เกิดจากการเรืองแสงและสีส้มแดงที่ได้รับเมื่อสัมผัสกับไฟฟ้า ใช้เพื่อวัตถุประสงค์ในการโฆษณา พบได้ง่ายในไฟนีออน. คุณยังสามารถซื้อหลอดนีออนและโคมไฟที่มีสีอื่นๆ ได้ แม้ว่าจริงๆ แล้วข้างในนั้นจะมีก๊าซอื่นๆ
- อาร์กอน: ก๊าซนี้ใช้ในหลอดไส้เพราะไม่ทำปฏิกิริยากับไส้หลอดภายใต้สภาวะที่มีอุณหภูมิและความดันสูง ในหลอดฟลูออเรสเซนต์จะสร้างสีเขียวน้ำเงิน นอกจากนี้ยังใช้ในอุตสาหกรรมเพื่อหลีกเลี่ยงปฏิกิริยาเคมีที่ไม่พึงประสงค์
- คริปทอน: ใช้ร่วมกับก๊าซอื่นๆ ในการสร้างและผลิตหลอดไฟ แสงสว่างที่สนามบินเนื่องจากความเข้มของแสงสีแดงที่ปล่อยออกมา; สามารถใช้ในเครื่องฉายภาพยนตร์ได้ การใช้คริปทอนยังมีประโยชน์ในการผ่าตัดม่านตาด้วยเลเซอร์
- ซีนอน: การใช้งานหลักของซีนอนคือการปรับปรุงรายละเอียดของตัวปล่อยแสงที่มีลักษณะการฆ่าเชื้อแบคทีเรีย หลอดเรืองแสง แฟลชถ่ายภาพ และในหลอดฟลูออเรสเซนต์ที่มีความสามารถในการกระตุ้นเลเซอร์ทับทิม
- เรดอน: ก๊าซนี้เกิดจากการสลายกัมมันตภาพรังสีของยูเรเนียมสู่คลื่นวิทยุ ด้วยเหตุนี้และเนื่องจากมีกัมมันตภาพรังสีสูงจึงมีการใช้งานในชีวิตประจำวันน้อยมาก
เพื่อไตร่ตรอง
แม้ว่าพวกเขาจะแต่งบ้าง หาได้ยากในสภาพธรรมชาติ (ยกเว้นฮีเลียมบางที) และเนื่องจากพวกมันสร้างหรือยอมให้ทำปฏิกิริยากับพวกมันค่อนข้างน้อย ก๊าซมีตระกูลจึงเป็นสารประกอบสำคัญที่เราสามารถมองเห็นได้ และแม้กระทั่งใช้ในชีวิตประจำวัน
บางทีการใช้งานอาจถูกจำกัดเฉพาะบางสาขา แต่นั่นไม่ได้หมายความว่าจะไร้ประโยชน์โดยสิ้นเชิง ตั้งแต่การให้แสงสว่างในบ้านของเราด้วยหลอดไฟและโคมไฟ ไปจนถึงการเก็บอาหารของเราไว้ใช้ในตู้เย็น ถึง ช่วยชีวิตเมื่อใช้ในการแพทย์ก๊าซธรรมชาติหรือสารสังเคราะห์เหล่านี้ยังไม่ได้แสดงสิ่งที่สามารถทำอะไรให้เราได้ และแน่นอนว่าในขณะที่การวิจัยดำเนินไป การใช้งานจะมีมากขึ้น
ความสามารถในการแตกตัวเป็นไอออนคืออะไร?
และความเปราะบางของมัน