மனித கண்ணுக்குத் தெரியாத சிறிய துகள்களால் மேட்டர் உருவாக்கப்பட்டுள்ளது, அவை அணுக்கள் மற்றும் மூலக்கூறுகள் என்று அழைக்கப்பட்டன, அவை இன்று நாம் அறிந்தவற்றின் முக்கிய கூறுகளாக இருக்கின்றன.
மேற்கூறிய துகள்கள் பொதுவாக இருக்கும் வேதியியல் பிணைப்பு எனப்படும் பிணைப்பு செயல்முறையை உள்ளிடவும், இவை நமக்கு முன்னால் தினமும் நிகழும் ஆயிரக்கணக்கான உயிரியல் செயல்முறைகளைப் புரிந்து கொள்வதற்காக வேதியியலால் ஆய்வு செய்யப்படுகின்றன, ஆனால் அதை எளிதில் உணர முடியாது. அவர்கள் மூலம்தான் உலகை எப்படியாவது மாற்றியமைக்கும் பெரும்பாலான நிகழ்வுகளை அவர்கள் புரிந்து கொள்ள முடிந்தது.
இரசாயன பிணைப்புகள் என்றால் என்ன?

மனிதர்கள் உட்பட உலகில் தற்போதுள்ள அனைத்து பொருட்களும், சில அணுக்கள் மற்றும் மூலக்கூறுகளின் ஒன்றிணைப்பால் ஆனவை, அவை ஒரு வேதியியல் பிணைப்பு எனப்படும் ஒரு செயல்முறையின் மூலம் சேர முடிவு செய்கின்றன. அனைத்து உயிரினங்களும் மந்தமான பொருட்களும் (உயிரற்ற பொருள்கள்) கூட பொருளால் ஆனவை என்பது அனைவரும் அறிந்ததே, மேலும் இது தன்னை உருவாக்கிக் கொள்ளக்கூடிய இரசாயன பிணைப்புகளைப் பொறுத்தது.
அணுக்கள் மற்றும் மூலக்கூறுகள் எவ்வாறு இணைக்கப்படுகின்றன என்பதைப் பொறுத்து, எந்த வகையான இரசாயன பிணைப்பு சிகிச்சையளிக்கப்படுகிறது என்பதை தீர்மானிக்க முடியும், மேலும் மிகவும் பொதுவானவற்றில் அயனி, கோவலன்ட் மற்றும் உலோக பிணைப்புகளைக் காணலாம், இருப்பினும் இரண்டு வகையான பிணைப்புகள் கண்டுபிடிக்கப்பட்டுள்ளன. ஹைட்ரஜன் பிரிட்ஜ் பிணைப்புகள் மற்றும் வான் டெர் வால்ஸ் ஆகியவை இந்த விஷயத்திற்கு வரும்போது நன்கு அறியப்படாத பத்திரங்கள்.
இரசாயன பிணைப்புகள் இரண்டு அல்லது அதற்கு மேற்பட்ட அணுக்களை ஒரு குறிப்பிட்ட காலத்திற்கு ஒன்றாக வைத்திருக்கச் செய்யும் சக்திகள் என்று அழைக்கப்படுகின்றன, மேலும் அவற்றுக்கிடையே எலக்ட்ரான்கள் பரவுவதை அனுமதிக்கின்றன.
இரண்டு அணுக்களுக்கு இடையில் நிகழும் ஈர்ப்பு செயல்முறை கொஞ்சம் விசித்திரமானது, ஆனால் கொஞ்சம் கவனத்துடன் பகுப்பாய்வு செய்தால் மிக எளிதாக புரிந்து கொள்ள முடியும். தெரிந்து கொள்ள வேண்டிய முக்கிய விஷயம் என்னவென்றால், நேர்மறை கட்டணங்களைக் கொண்ட கருக்கள் விலகிச் செல்கின்றன, ஆனால் அதே நேரத்தில் அவை எலக்ட்ரான்களுக்கு அவற்றின் மேற்பரப்பில் இருக்கும் எதிர்மறை கட்டணத்துடன் நன்றி செலுத்தப்படலாம், இது பல சந்தர்ப்பங்களில் அது செய்யும் சக்தியை விட அதிகமாக இருக்கும் கருக்கள் விலகிச் செல்ல காரணமாகிறது.
வேதியியல் பிணைப்பு செயல்முறை வழக்கமாக நிகழும்போது, எல்லா நேரத்திலும் இல்லை சில அணுக்கள் எலக்ட்ரான்களை இழக்கின்றன மற்றவர்கள் வெற்றி பெறுகிறார்கள், ஆனால் செயல்பாட்டின் முடிவில் அனைத்து செயல்களிலும் மின் நிலைத்தன்மையைக் காணலாம்.
5 வகையான இரசாயன பிணைப்புகள்
அவை எவ்வாறு செயல்படுகின்றன என்பதைப் புரிந்துகொள்வதற்காக ரசாயன பிணைப்புகள் மற்றும் அவற்றின் சில பண்புகள் கீழே காட்டப்படும்.

உலோக இணைப்புகள்
இந்த வகை பிணைப்பில், முழு அணுக்களின் தொகுப்பையும் ஒன்றாக வைத்திருக்கும் ஒரு மேகம் எவ்வாறு உருவாக்கப்படுகிறது என்பதைக் காணலாம், இது தளர்வான எலக்ட்ரான்களால் உருவாகிறது. இந்த செயல்பாட்டில் அணுக்கள் எலக்ட்ரான்கள் மற்றும் அயனிகளாக எவ்வாறு மாற்றப்படுகின்றன என்பதைக் காணலாம், இது சாதாரணமாக நடப்பதற்குப் பதிலாக, அருகிலுள்ள அணுவை விட்டு விடுகிறது.
உலோக பிணைப்புகள் பொதுவாக படிகமாகக் கருதப்படும் நெட்வொர்க்குகளை உருவாக்குகின்றன, அவை அதிக ஒருங்கிணைப்புக் குறியீட்டைக் கொண்டுள்ளன.
இந்த நெட்வொர்க்குகளின் முகங்களில் நீங்கள் மூன்று வெவ்வேறு வகையான படிக நெட்வொர்க்குகளைக் காணலாம், அவை வெவ்வேறு ஒருங்கிணைப்பு புள்ளிகளைக் கொண்டுள்ளன, அவை இருக்கும் இடத்தைப் பொறுத்து மாறுகின்றன, 12 புள்ளிகள், 8 புள்ளிகள் மற்றும் கடைசியாக 6 புள்ளிகளுடன் அடையும், இருப்பினும், உலோக அணுக்களின் வேலன்ஸ் நிலை எப்போதும் சிறியது.
அயனி பிணைப்புகள்
அயனி பிணைப்புகளைப் பற்றி நாம் பேசும்போது, சிறிய மின்னாற்பகுப்பு ஆற்றலைக் கொண்ட அணுக்களுக்கிடையேயான ஒன்றியத்தைக் குறிக்க விரும்புகிறோம், அவை முதல் வகைகளை விட ஒரே மாதிரியான ஆற்றலைக் கொண்டவை, அவை பொதுவாக உலோக உறுப்பு மற்றும் உலோகமற்ற உறுப்பு . இது நடக்க, அணுக்களில் ஒன்று எலக்ட்ரான்களை இழக்க வேண்டியது அவசியம், மற்றொன்று தொடர்ச்சியாக அவற்றைப் பெற முடியும். ஆகையால், இந்த பிணைப்பை இரண்டு அணுக்கள் ஒரு மின்னியல் ஈர்ப்பைக் கொண்ட ஒரு செயல்முறையாக விவரிக்கப்படலாம், இதில் ஒன்று அதிக ஈர்ப்புடனும் மற்றொன்று குறைந்த ஈர்ப்புடனும் பங்கேற்கிறது.
உலோகம் அல்லாத கூறுகள் அவற்றின் முழுமையான சுற்றுப்பாதையை வைத்திருக்க அவற்றின் கலவையில் ஒரு எலக்ட்ரான் இல்லை என்று காட்டப்பட்டது, இந்த காரணத்தினால்தான் இது செயல்முறையின் பெறுநராக மாறுகிறது, இது ஒரு அயனி என அழைக்கப்படுகிறது.
உலோகக் கூறுகள் கேஷன்ஸ் என்று அழைக்கப்படுகின்றன, ஏனெனில் அவை அனான்களுக்கு நேர்மாறான நேர்மறையான கட்டணம் இருப்பதால், அவற்றின் கலவையின் கடைசிப் பகுதியில் எலக்ட்ரான் இருப்பதால், அவை மற்ற அணுக்களுடன் பிணைக்கும் திறனைக் கொண்டுள்ளன, இந்த விஷயத்தில் உலோகமற்றவை.
விவரிக்கப்பட்டுள்ளவற்றால் வழிநடத்தப்பட்டால், இந்த வகை இரசாயன பிணைப்பில் அணுக்கள் ஒரு மின்னியல் சக்தியால் ஈர்க்கப்படுகின்றன, எனவே அயனி கேஷனை ஈர்க்கிறது, மேலும் அணுக்களில் ஒன்று விளைவிக்கும் போது அதைக் கவனிக்க முடியும். மற்றது உறிஞ்சும் போது. இந்த கலவை திடமாக இருக்கும்போது, அது விவரிக்கப்பட்டதாகவும் நிலையானதாகவும் இருக்கும், ஆனால் துல்லியமான தருணத்தில் அது ஈரப்பதமான சூழலில் அல்லது இயல்புநிலையாக சில திரவத்தில் வைக்கப்படுகிறது, அவை மீண்டும் பிரிந்து, அவற்றின் மின் கட்டணங்களை பராமரிக்கின்றன.
பங்கீட்டு பிணைப்புகள்
கோவலன்ட் பிணைப்புகளில், அணுக்கள் எலக்ட்ரான்களை ஈர்க்கவும் பகிர்ந்து கொள்ளவும் அல்லது மேலே குறிப்பிட்ட நிகழ்வுகளைப் போல அவற்றை உறிஞ்சும் திறனைக் கொண்டுள்ளன, மேலும் இவை நிகழும்போது அயனிகள் மிகவும் நிலையானவை என்று நிரூபிக்கப்பட்டுள்ளது.
பெரும்பாலான இணைப்புகள் மின்சாரத்தை கடத்தும் திறன் கொண்டவை என்று கூறலாம், ஆனால் இந்த விஷயத்தில் ஒரு பெரிய பகுதி இல்லை என்று மாறிவிடும். எல்லா கரிமப் பொருட்களும் கோவலன்ட் பிணைப்புகளால் ஆனவை, ஏனெனில் மேலே குறிப்பிட்டுள்ளபடி இது மிகவும் நிலையானது.
இந்த பிணைப்புகள் அவற்றின் சொந்த பிரிவைக் கொண்டுள்ளன, இது ஒரு தூய்மையான கலவையா இல்லையா என்பதைப் பொறுத்து மாறுபடும், அவை துருவப் பிணைப்புகள் என்று அழைக்கப்படுகின்றன மற்றும் துருவமற்றவை என்று சுருக்கமாக விளக்கம் கீழே கொடுக்கப்படும்.
துருவ கோவலன்ட் பிணைப்பு
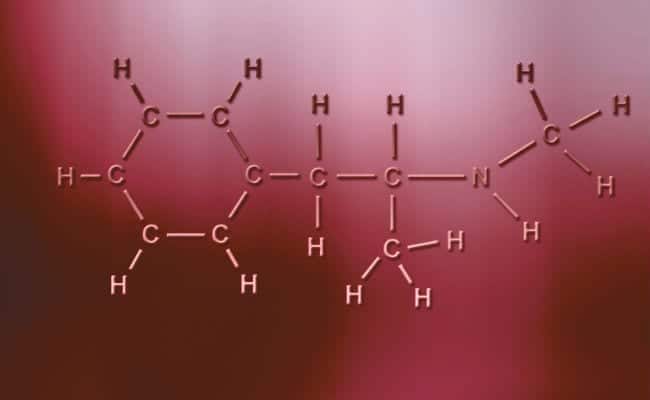
துருவ கோவலன்ட் பிணைப்புகளின் முக்கிய பண்பு என்னவென்றால், அவை முற்றிலும் சமச்சீரற்றவை, அதாவது நேர்மறை அல்லது எதிர்மறை கட்டணம் கொண்ட அணுக்கள் பகிர்ந்து கொள்ள இரண்டு எலக்ட்ரான்கள் அல்லது உறிஞ்சுவதற்கு இரண்டு இடைவெளிகளைக் கொண்டிருக்கலாம், மற்றொன்று ஒன்று மட்டுமே உள்ளது, வழக்குகள் மாறுபடும். இவை நடைமுறையில் அயனி பிணைப்புகளைப் போலவே நிகழ்கின்றன, ஆனால் அணுக்கள் ஒன்றிணைவதற்கான ஒரே வித்தியாசத்துடன், ஒரு துருவ கோவலன்ட் பிணைப்பு ஏற்படுகிறது. இவை நிகழ, அவை முற்றிலும் வேறுபட்ட இரண்டு உலோகமற்ற கூறுகளுக்கு இடையில் நிகழ வேண்டும்,
அல்லாத துருவ கோவலன்ட் பிணைப்பு
மேலே விவரிக்கப்பட்ட வேதியியல் பிணைப்பு வகையைப் போலன்றி, இந்த விஷயத்தில் ஒரே மாதிரியான ஒரு அல்லாத அளவிலான இரண்டு அல்லது அதற்கு மேற்பட்ட அணுக்கள் இருக்க வேண்டும். இது ஒவ்வொரு வகையிலும் துருவத்திலிருந்து முற்றிலும் வேறுபட்டது, மேலும் ஒரே உறுப்பின் இரண்டு அணுக்கள் எலக்ட்ரான்களைப் பகிர்ந்து கொள்ளும்போது, அவை முற்றிலும் சமச்சீராக இருக்கும்போது, அவை சீரானதாக இருப்பதோடு, எலக்ட்ரான்களை சமமாகப் பெற்று நன்கொடை அளிக்கின்றன என்பதை அறிந்து கொள்வதன் மூலம் இதை நிரூபிக்க முடியும்.
ஹைட்ரஜன் பிணைப்பு பிணைப்புகள்
ஹைட்ரஜன் எப்பொழுதும் நேர்மறையான கட்டணத்தைக் கொண்டிருப்பதன் மூலம் வகைப்படுத்தப்படுகிறது, மேலும் இந்த பிணைப்பைச் செய்வதற்கு இது ஒரு எலக்ட்ரோநெக்டிவ் சார்ஜ் கொண்ட ஒரு அணுவால் ஈர்க்கப்பட வேண்டியது அவசியம், இது இந்த செயல்முறைக்கு நன்றி ஒரு இடையே ஒரு தொழிற்சங்கம் எவ்வாறு உருவாகிறது என்பதைக் காணலாம் ஒரு ஹைட்ரஜன் பாலம் போல குறிப்பிடப்பட்ட ஒன்றில் இரண்டு, பிணைப்பின் பெயர் பெறப்பட்ட இடத்திலிருந்து.
வான் டெர் வால்ஸுக்கான இணைப்புகள்
இந்த வகை இணைப்புகளில், இரண்டு நிரந்தர இருமுனைகளுக்கிடையேயான ஒன்றியம், அதே போல் இரண்டு தூண்டப்பட்ட இருமுனைகளுக்கு இடையில் காணப்படுகிறது, அல்லது ஒரு நிரந்தர மற்றும் தூண்டப்பட்ட இருமுனைக்கு இடையில் தொழிற்சங்கங்கள் காணப்படுவதற்கான வாய்ப்பு இருக்கலாம். இது நிகழ ஒரே வழி இரண்டு சமச்சீர் மூலக்கூறுகளுக்கு இடையில் உள்ளது, அவை மூலக்கூறுகளுக்கு இடையில் ஒரு ஈர்ப்பு அல்லது விரட்டல் இருக்கும்போது அல்லது இயல்பாகவே அயனிகள் மற்றும் மூலக்கூறுகளுக்கு இடையிலான தொடர்பு இருக்கும்போது செயல்படத் தொடங்குகின்றன.
நிலையான ஆய்வுக்கு நன்றி தற்போதுள்ள அனைத்து வகையான இரசாயன பிணைப்புகளுக்கும் பொருந்தும் இந்த செயல்முறைகளில் பெரும்பாலானவற்றில் விவரிக்கப்பட்டுள்ளபடி எலக்ட்ரான் பரிமாற்ற நடவடிக்கையில் மாற்றப்பட்ட பின்னர் விஷயம் எவ்வாறு இயங்குகிறது மற்றும் அதை முற்றிலும் புதிய தயாரிப்பாக மாற்றுவது அல்லது அதன் வடிவத்திற்கு திரும்புவது எப்படி என்பதை இன்னும் கொஞ்சம் புரிந்துகொள்ள முடிந்தது.
தொழில்நுட்பத்தின் முன்னேற்றத்திற்கு நன்றி இந்த அறிவு அனைத்தும் அடையப்பட்டுள்ளது, இதற்கு முன்னர் இது அணுக்களின் இருப்பைப் பற்றி மட்டுமே ஊகிக்கப்பட்டது, இதற்கு ஒரு எடுத்துக்காட்டு சிறந்த தத்துவ சிந்தனையாளர்களின் அணு மாதிரிகள் இருப்பதே ஆகும், இருப்பினும் அவை இதுவரை இல்லை இன்று அறியப்படுகிறது, இன்று செயல்முறைகளை நன்கு புரிந்துகொள்ள முடிந்தது.